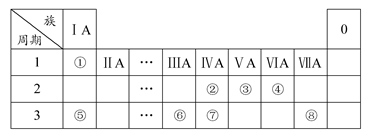
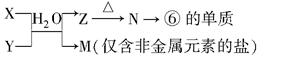题目内容
下列陈述I、II均正确并且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | Fe3+有氧化性 | 铁盐可用作净水剂 |
| B | SiO2是两性氧化物 | SiO2可和HF反应 |
| C | Al2O3的熔点很高 | Al2O3可用作耐火材料 |
| D | SO2有漂白性 | SO2可使高锰酸钾溶液褪色 |
C
解析试题分析:陈述I、II均正确,但无因果关系,铁盐用作净水剂的原因是铁离子水解生成氢氧化铁胶体,而非铁离子的氧化性,故A错误;陈述I错误,陈述II正确,因为二氧化硅是酸性氧化物,不能溶于HF之外的酸,故B错误;陈述I、II正确,且有因果关系,故C正确;陈述I、II均正确,但是无因果关系,二氧化硫有漂白性是它能使品红溶液褪色的原因,二氧化硫有还原性是它可使高锰酸钾溶液褪色的原因,故D错误。
考点:元素化合物的主要性质及应用,涉及铁离子的水解反应及应用、二氧化硅的性质、氧化铝的熔点及应用、二氧化硫的漂白性和还原性及应用等。

练习册系列答案
相关题目
用如图所示装置进行下列实验,足量时间后,实验结果与预测的现象不一致的是
| | ① | ② | 预测的现象 |
| A | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
| B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
| C | AlCl3溶液 | 浓氨水 | 有白色沉淀 |
| D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
下列各组物质中,物质之间通过一步反应就能实现图示变化的是
| 物质编号 | 物质转化关系 | a | b | c | d |
| ① |  | FeCl2 | FeC13 | Fe | CuCl2 |
| ② | NO | NO2 | N2 | HNO3 | |
| ③ | Na2O | Na2O2 | Na | NaOH | |
| ④ | Al2O3 | NaAlO2 | Al | Al(OH)3 |
A.①④ B.①②③ C.①③④ D.②④
下列物质的转化在给定条件下能实现的是
①氯化钠饱和溶液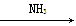
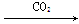 NaHCO3(s)
NaHCO3(s)
②N2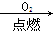 NO2
NO2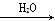 HNO3
HNO3
③海水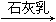 Mg(OH)2
Mg(OH)2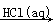 MgCl2(aq)
MgCl2(aq) MgCl2(s)
MgCl2(s)
④Al2O3 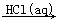 AlCl3(aq)
AlCl3(aq) 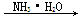 Al(OH)3
Al(OH)3
⑤重晶石(BaSO4) 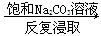 BaCO3
BaCO3 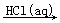 BaCl2(aq)
BaCl2(aq)
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
下列叙述正确的是
| A.钠在空气中燃烧生成淡黄色的Na2O2 |
| B.将SO2通入过量BaCl2溶液可生成BaSO3沉淀 |
| C.新制氯水显酸性,向其中滴加少量紫色石蕊试液,振荡后溶液最终呈红色 |
| D.点燃的镁条插入盛有CO2的集气瓶中,立即熄灭 |
根据下列实验现象得出的结论,正确的是
| 选项 | 实验现象 | 结论 |
| A | 某气体能使润湿的淀粉碘化钾试纸变蓝 | 该气体一定是氯气 |
| B | 向某溶液中加入盐酸酸化的BaCl2,有白色沉淀生成 | 该溶液中一定存在SO42- |
| C | 铁与稀硝酸充分反应后,溶液呈浅绿色 | 稀硝酸与铁反应只能生成Fe2+ |
| D | SO2通入溴水中,溴水褪色 | SO2具有还原性 |
从下列事实所得出的相应结论正确的是
| | 实验事实 | 结论 |
| A | 氢氧化铝可以溶解在氢氧化钠溶液中 | 氢氧化铝属于碱 |
| B | CO2的水溶液可导电 | CO2是电解质 |
| C | SO2通入酸性高锰酸钾溶液,溶液褪色 | SO2有漂白性 |
| D | 铁分别和氯气、硫反应得到氯化铁和硫化亚铁 | 氯气的氧化性大于硫 |
对下列实验现象的描述不正确的是
| A.光亮的金属Na暴露在空气中,表面逐渐变暗 |
| B.将SO2通入品红溶液,品红溶液褪色 |
| C.将Mg(OH)2固体投入FeCl3溶液中,无明显现象 |
| D.浓硫酸与Cu混合加热,可能有白色固体析出 |