题目内容
某无色气体可能含有H2S、SO2、CO2、HI、HCl气体中的一种或几种.将气体通入氯水后,得无色溶液,向该溶液中滴加氯化钡溶液,有白色沉淀产生.则下列叙述正确的是( )
| A.该气体中肯定含有H2S和SO2 |
| B.该气体中肯定含有SO2 |
| C.该气体中肯定含有CO2和SO2 |
| D.该气体中肯定含有H2S、CO2和HI |
氯水为黄绿色,将气体A通入氯水中得无色透明溶液,说明溶液中一定有SO2,因为SO2+Cl2+2H2O═2HCl+H2SO4;一定无H2S,因为2H2S+SO2═3S↓+2H2O,SO2和H2S不共存;一定无HI,因为2HI+Cl2═I2+2HCl,生成的I2微溶,且碘水呈褐色.向溶液中加入BaCl2溶液产生白色沉淀,进一步证明有SO2气体.
故选B.
故选B.

练习册系列答案
相关题目
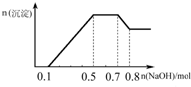 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )| A、溶液中的阳离子只有H+、Mg2+、Al3+ | B、溶液中n(NH4+)=0.2mol | C、溶液中一定不含CO32-,可能含有SO42-和NO3- | D、三种离子的物质的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1 |
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法正确的是( )

