题目内容
2.下列关于反应热的说法正确的是( )| A. | 已知C(石墨,s)═C(金刚石,s)△H﹦+1.9kJ•mo1-1,说明金刚石具有的能量比石墨低 | |
| B. | 已知H+(aq)+OH-(aq)═H2O(1)△H﹦-57.4KJ•mo1-1,20g氢氧化钠固体溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ | |
| C. | 已知甲烷的燃烧热为890.3kJ•mo1-1,则表示甲烷燃烧热的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H﹦-890.3kJ•mo1-1 | |
| D. | 将0.5mo1N2和1.5mo1H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H﹦-38.6kJ•mo1-1 |
分析 A.石墨转化为金刚石吸热,金刚石能量大于石墨的总能量;
B.氢氧化钠固体溶解过程中放热;
C.燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物的过程中放出热量,气态水不是稳定态;
D.根据反应是可逆反应不能进行彻底和焓变意义分析判断.
解答 解:A.吸热反应反应物的总能量低于生成物的总能量,C(石墨,s)═C(金刚石,s)△H﹦+1.9kJ•mo1-1<0,可知反应时吸热,金刚石能量高于石墨,故A错误;
B.氢氧化钠固体溶解过程中放热,20g氢氧化钠固体物质的量为0.5mol,溶于稀盐酸中恰好完全反应时放出的热量大于28.7kJ,故B正确;
C.甲烷的标准燃烧热为-890.3kJ•mo1-1,燃烧热概念是1mol可燃物完全燃烧生成稳定氧化物的过程中放出热量,甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mo1-1,故C错误;
D.反应是可逆反应不能进行彻底,将0.5mo1N2和1.5mo1H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,焓变是指对应物质量下完全反应放出的热量,反应其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H<-38.6kJ•mo1-1 ,故D错误;
故选B.
点评 本题考查了化学反应能量变化有关知识,注意燃烧热、中和热概念分析判断,注意反应可逆反应不能进行彻底,题目难度中等.

练习册系列答案
相关题目
13.设NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | NA个N2分子和NA个CO2原子个数比为1:1 | |
| B. | 1 mol H2O的质量与NA个H2O质量的总和几乎相等 | |
| C. | 1mol H2所含的原子数为NA | |
| D. | 1mol H2SO4中所含的粒子数目一定是NA |
7.如表相关实验不能达到预期目的是( )
| 相关实验 | 预期目的 | |
| A | 试样加水溶解后,再加入足量Ca(OH)2溶液,有白色沉淀生成 | 检验NaHCO3固体中是否含 Na2CO3 |
| B | 向少量燃尽火柴头的浸泡液中滴加足量稀HNO3、AgNO3 | 验证火柴头含有氯元素 |
| C | 加入饱和Na2CO3溶液,充分振荡,静置、分层后,分液 | 除去乙酸乙酯中的乙酸 |
| D | 两支试管中装有等体积、等浓度的 H2O2溶液,向其中一支试管中加入 FeCl3溶液 | 探究FeCl3溶液对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
11.美、德两国成功合成具有化学特性的氢铝化合物(AlH3)n,关于氢铝化合物的推测不正确的是( )
| A. | 氢铝化合物与水反应生成氢氧化铝和氢气 | |
| B. | 氢铝化合物中铝显+3价,氢显-1价 | |
| C. | 铝与水蒸气高温下反应生成氢铝化合物 | |
| D. | 氢铝化合物具有强还原性 |
12.为提纯下列物质(括号内为杂质),选用的试剂或方法有错误的是( )
| 物质 | 试剂 | 分离方法 | |
| A | 硝酸钾(氯化钠 ) | 蒸馏水 | 降温结晶 |
| B | 氢氧化铁胶体(Fe3+) | 蒸馏水 | 渗析 |
| C | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
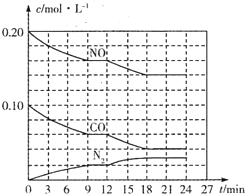 为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.
为有效控制雾霾,各地积极采取措施改善大气质量.有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质.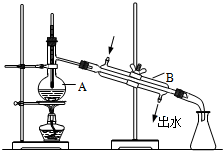 如图为实验室制取蒸馏水的装置示意图,请根据图示回答下列问题.
如图为实验室制取蒸馏水的装置示意图,请根据图示回答下列问题.