题目内容
下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A、1molH2O含有的H2O分子数目为NA |
| B、1molH2O含有的原子数目为3NA |
| C、32克O2所含的原子数目为NA |
| D、通常状况下,11.2L氮气含氮分子数目为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据N=n?NA来计算;
B、根据1mol水中含3mol原子来分析;
C、氧气为双原子分子,1mol氧气含有2mol氧原子;
D、通常状况下,气体摩尔体积不是22.4L/mol.
B、根据1mol水中含3mol原子来分析;
C、氧气为双原子分子,1mol氧气含有2mol氧原子;
D、通常状况下,气体摩尔体积不是22.4L/mol.
解答:
解:A、根据N=n?NA可知1mol水中含NA个水分子,故A正确;
B、1mol水中含3mol原子,故原子数为3NA,故B正确;
C、32g氧气的物质的量是1mol,所以含有2mol氧原子,所含的原子数目为2NA,故C错误;
D、通常状况下,气体摩尔体积大运22.4L/mol,故11.2L氮气的物质的量小于0.5mol,故含有的分子数目小于0.5NA,故D错误.
故选CD.
B、1mol水中含3mol原子,故原子数为3NA,故B正确;
C、32g氧气的物质的量是1mol,所以含有2mol氧原子,所含的原子数目为2NA,故C错误;
D、通常状况下,气体摩尔体积大运22.4L/mol,故11.2L氮气的物质的量小于0.5mol,故含有的分子数目小于0.5NA,故D错误.
故选CD.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案
相关题目
下列说法正确的是( )
| A、能电离出H+的化合物叫做酸 |
| B、实验测得1mol某气体体积为22.4L,测定条件一定是标准状况 |
| C、摩尔是七个基本物理量之一 |
| D、用树状分类法可以将化合物分类为酸、碱、盐和氧化物 |
Rm+与Xn-具有相同的电子层结构,则微粒半径( )
| A、前者大于后者 |
| B、前者小于后者 |
| C、前者等于后者 |
| D、大小比较不能确定 |
在相同条件下,下列气体中与14gN2具有相同分子数目的是( )
| A、32g O2 |
| B、15g NO |
| C、34g NH3 |
| D、80g Ar |
下列关于化学用语的表示正确的是( )
A、过氧化钠的电子式: | ||
B、质子数为35、中子数为45的溴原子:
| ||
| C、氯化铵、次氯酸都属于强电解质 | ||
| D、只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 |
物质分类是化学研究的重要方法之一,下列物质分类的正确组合是( )
| 混合物 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 液氧 | 苛性钠 | 胆矾[ | 氧化铁 | 二氧化碳 |
| B | 盐酸 | 烧碱 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 碘酒 | 纯碱 | 石灰石 | 氨气 | 水 |
| D | 大理石 | 熟石灰 | 纯碱 | 生石灰 | 二氧化硫 |
| A、A | B、B | C、C | D、D |
下列属于阴离子的是( )
A、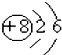 |
B、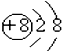 |
C、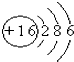 |
D、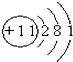 |
在下列溶液中,各组离子一定能够大量共存的是( )
| A、在含有NaHCO3的溶液中:K+、SO42-、Cl-、Al3+ |
| B、使甲基橙变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
| C、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- |
| D、水电离的c(H+)=10-11 mol?L-1的溶液:NH4+、K+、ClO-、Cl- |