题目内容
下列物质中,既属于电解质又能导电的是( )
分析:电解质是指在水溶液中或熔融状态下能导电的化合物,例如酸、碱和盐等,凡在上述情况下不能导电的化合物叫非电解质,例如蔗糖和酒精等.注意电解质和非电解质都是化合物,既要排除单质又要排除混合物.
解答:解:A、二氧化硫的水溶液能导电,但电离出自由移动离子的是亚硫酸不是二氧化硫,所以二氧化硫不是电解质,故A正确;
B、NaOH溶液有自由移动的离子,能导电,属于混合物,则既不是电解质也不是非电解质,故B错误;
C、石墨是能导电的非金属单质不是化合物,既不是电解质也不是非电解质,故C错误.
D、因为熔融的KNO3含有自由移动的离子能导电,所以熔融状态的氯化钠是能导电的电解质,故D正确;
故选:D;
B、NaOH溶液有自由移动的离子,能导电,属于混合物,则既不是电解质也不是非电解质,故B错误;
C、石墨是能导电的非金属单质不是化合物,既不是电解质也不是非电解质,故C错误.
D、因为熔融的KNO3含有自由移动的离子能导电,所以熔融状态的氯化钠是能导电的电解质,故D正确;
故选:D;
点评:本题考查了电解质和非电解质的判断,难度不大,注意不是电解质的物质不一定是非电解质,如:单质、混合物既不是电解质也不是非电解质.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
[化学-选修物质结构与性质]
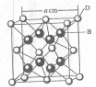
已知A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期也不在同一主族.B原子的L层有1对成对电子且其单质是空气的主要成分.C原子的L层p轨道中有5个电子;D是周期表中1--18列中的第14列元素;D元素原子次外层电子数与最外层电子数之比为4:1. E跟C可形成离子化合物,其晶胞结构如右图.请回答:
(1)A与D形成的最简单化合物的分子式是 ,该分子的立体构型是 .该分子属于 (填“极性”或“非极性”)分子
(2)C与D形成的化合物晶体类型是 .B单质分子中含 个σ键 个π键
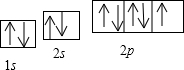
(3)C的电子排布图
(4)从上图中可以看出,E踉C形成的化合物的化学式为 ;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是 (只要求列出算式).
(5)电负性(用X表示)也是元素的一种重要性质,下表给出8种元素的电负性数值:
请回答下列有关问题:
①估计钙元素的电负性的取值范围: <X<
②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于17时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlC13中形成的化学键的类型及其理由是 .

已知A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期也不在同一主族.B原子的L层有1对成对电子且其单质是空气的主要成分.C原子的L层p轨道中有5个电子;D是周期表中1--18列中的第14列元素;D元素原子次外层电子数与最外层电子数之比为4:1. E跟C可形成离子化合物,其晶胞结构如右图.请回答:
(1)A与D形成的最简单化合物的分子式是 ,该分子的立体构型是 .该分子属于 (填“极性”或“非极性”)分子
(2)C与D形成的化合物晶体类型是 .B单质分子中含 个σ键 个π键
(3)C的电子排布图
(4)从上图中可以看出,E踉C形成的化合物的化学式为 ;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是 (只要求列出算式).
(5)电负性(用X表示)也是元素的一种重要性质,下表给出8种元素的电负性数值:
| 元素 | Na | Mg | Al | Si | P | S | Cl | K |
| 电负性 | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | 0.8 |
①估计钙元素的电负性的取值范围: <X<
②经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于17时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlC13中形成的化学键的类型及其理由是 .

 (2011?咸阳模拟)[化学-选修物质结构与性质]
(2011?咸阳模拟)[化学-选修物质结构与性质]