题目内容
下列反应在容器中建立化学平衡:SO2+NO2?NO+SO3,若在容器中通入一定量的O2,此时反应将会发生的变化是( )
分析:反应SO2(g)+NO2(g)?NO(g)+SO3(g),达到平衡状态后,加入一定量的氧气,氧气与一氧化氮反应生成了二氧化氮,导致一氧化氮浓度减小,二氧化氮浓度增大,所以化学平衡向着正向移动,据此进行判断.
解答:解:由于反应SO2(g)+NO2(g)?NO(g)+SO3(g),达到平衡状态后,加入一定量的氧气,氧气与一氧化氮反应生成了二氧化氮,导致一氧化氮浓度减小,二氧化氮浓度增大,所以化学平衡向着正向移动,
故选A.
故选A.
点评:本题考查了化学平衡的影响因素,注意分析题中信息,根据平衡移动原理进行分析,题目较简单.

练习册系列答案
相关题目
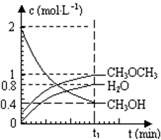 已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:
已知二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=23.5kJ?mol-1.在T1℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示.请回答下列问题:
 CH3OH(g) △H = —90.7kJ·mol—1
CH3OH(g) △H = —90.7kJ·mol—1 CH3OCH3(g)+CO2(g),则该反应的△H =
CH3OCH3(g)+CO2(g),则该反应的△H = 
 ,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
 、
、 此时正、逆反应速率的大小:
此时正、逆反应速率的大小: _______
_______ (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。

 2MgCl4+Ti在Ar气氛中进行的理由是____________________。
2MgCl4+Ti在Ar气氛中进行的理由是____________________。 CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
CH3OCH3(g)+H2O(g) ΔH=" -23.5" kJ/mol
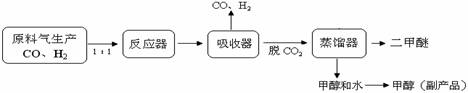
 CH3OH(g) △H =
—90.7kJ·mol—1
CH3OH(g) △H =
—90.7kJ·mol—1 CH3OCH3(g)+CO2(g),则该反应的△H
=
CH3OCH3(g)+CO2(g),则该反应的△H
=

 ,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
 、
、 此时正、逆反应速率的大小:
此时正、逆反应速率的大小: _______
_______ (填“>”、“<”、或“=”)。
(填“>”、“<”、或“=”)。