题目内容
对于反应3Cl2+6NaOH═5NaCl+NaClO3+3H2O,以下叙述正确的是( )
| A、Cl2是氧化剂,NaOH是还原剂 |
| B、被氧化的Cl原子和被还原的Cl原子的物质的量的比为1:5 |
| C、Cl2既是氧化剂又是还原剂 |
| D、每生成1mol的NaClO3转移6mol的电子 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:3Cl2+6NaOH═5NaCl+NaClO3+3H2O中,只有Cl元素的化合价变化,Cl元素的化合价由0降低为-1价,由0升高为+5价,以此来解答.
解答:
解:A.Cl元素的化合价由0降低为-1价,由0升高为+5价,Cl2是氧化剂也是还原剂,故A错误;
B.氯气化合价部分升高部分降低,既是氧化剂又是还原剂,化合价升高被氧化的Cl原子和化合价降低被还原的Cl原子的物质的量的比为1:5,故B正确;
C.Cl元素的化合价由0降低为-1价,由0升高为+5价,Cl2是氧化剂也是还原剂,故C正确;
D.由Cl元素的化合价升高可知,每生成1mol的NaClO3转移5mol的电子,故D错误;
故选BC.
B.氯气化合价部分升高部分降低,既是氧化剂又是还原剂,化合价升高被氧化的Cl原子和化合价降低被还原的Cl原子的物质的量的比为1:5,故B正确;
C.Cl元素的化合价由0降低为-1价,由0升高为+5价,Cl2是氧化剂也是还原剂,故C正确;
D.由Cl元素的化合价升高可知,每生成1mol的NaClO3转移5mol的电子,故D错误;
故选BC.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4L二氯甲烷的分子数约为NA个 |
| B、常温下,在18g18O2中含有NA个氧原子 |
| C、1.0L 1.0mo1?L-1的NaAlO2水溶液中含有的氧原子数为2NA |
| D、25℃时pH=13的NaOH溶液中含有OH一的数目为0.1NA |
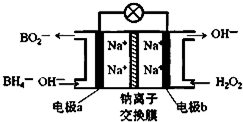 某新型电池NaBH4(其中B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境的电源,其工作原理如图所示.下列说法正确的是( )
某新型电池NaBH4(其中B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境的电源,其工作原理如图所示.下列说法正确的是( )| A、电池工作时Na+从b极区移向a极区 |
| B、b极上的电极反应式为:H2O2+2e-+2H+═2H2O |
| C、每消耗3molH2O2,转移3mol e- |
| D、a极上的电极反应式为:BH4-+8OH--8e-═BO2-+6H2O |
下列各项是关于玻璃棒在若干实验中的用途及操作,其中错误的是( )
①溶解物质时搅拌
②蒸发操作时搅拌液体防止暴沸
③蘸取少量溶液测其pH
④过滤时用玻璃棒引流,其下端在漏斗内滤纸的任意部位
⑤配制一定体积的物质的量浓度的溶液用玻璃棒引流
⑥加热坩埚中固体物质用玻璃棒翻炒固体.
①溶解物质时搅拌
②蒸发操作时搅拌液体防止暴沸
③蘸取少量溶液测其pH
④过滤时用玻璃棒引流,其下端在漏斗内滤纸的任意部位
⑤配制一定体积的物质的量浓度的溶液用玻璃棒引流
⑥加热坩埚中固体物质用玻璃棒翻炒固体.
| A、①③⑤ | B、③④⑥ |
| C、只有④ | D、全部错误 |
如图所示是短周期元素A、B、C在周期表中的位置,A、C两种元素的原子核外电子数之和等于B原子的核电荷数.下列说法正确的是( )
| A | C | |
| B |
| A、元素A和C的氢化物分子之间都存在氢键 |
| B、C原子的最外层电子数为6 |
| C、元素B只存在一种氧化物 |
| D、元素A有多种可变的化合价 |
下列实验操作中错误的是( )
| A、用试管加热液体时,所盛液体不超过容积的三分之一 |
| B、试剂瓶倾倒液体时,标签朝手心 |
| C、滴定时,眼睛注视滴定管中的液面 |
| D、称量时,腐蚀性固体药品要放在小烧杯或表面皿中 |
下列说法正确的是( )
| A、1molCO和1molN2所含分子数相等,质量相等,它们所占的体积也相等 |
| B、22.4LH2和71gCl2的物质的量相等 |
| C、非标准状况下,1mol任何气体的体积有可能是22.4L |
| D、1molHCl和1molH2O在标准状况下的体积都约是22.4L |