��Ŀ����
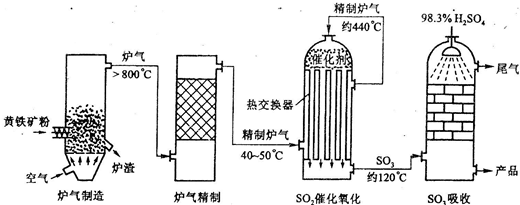
�Ի�����Ϊԭ����������Ĺ�������ͼ���£�
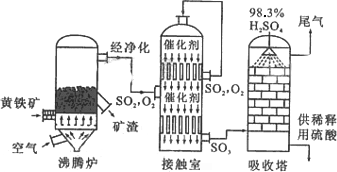
(1)��д������¯�л�����ȼ�յĻ�ѧ����ʽ��________________��
(2)�Ӵ�����2SO2(g)
��O2(g)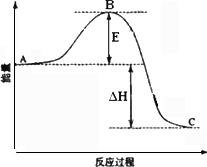
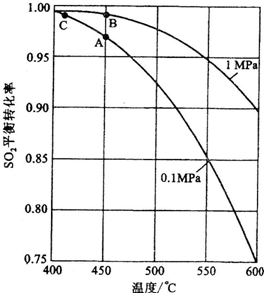
�����ݹ�������ͼ�ж�����˵����ȷ����(ѡ�������ĸ)________��
a��Ϊʹ��������ȼ�գ��轫�����
b���������������SO2��ת����
c��ʹ�ô��������SO2�ķ�Ӧ���ʺ�ת����
d������¯�ų��Ŀ����ɹ�����
�ڷ�Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK��________�������¶ȣ�Kֵ________(���������С�����䡱)��ͼ�С�H��________KJ��mol��1��
��ͼ��C���ʾ________��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ��________(��С����ޡ�)Ӱ�죮�÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B��________(����ߡ����͡�)��
�������Ӧ����v(SO2)Ϊ0.05 mol��L��1��min��1����v(O2)��________mol��L��1��min��1��
����֪�������ȼ����Ϊ��296 KJ��mol��1��������S(s)����3 mol��SO3(g)�ġ�H��________��
(3)�������ų���β�����ð�ˮ���գ�����Ũ���ᴦ�����õ��ϸ�Ũ�ȵ�SO2����Σ�SO2�ȿ���Ϊ���������ԭ��ѭ�������ã�Ҳ�����ڹ�ҵ������������ճ�ʪ�����е�Br2��SO2����Br2�����ӷ���ʽ��________________��
������
����(1)4FeS2
��11O2����(2)��a��b��d��(��2
�֣����2����1�֣����3����2�֣���������÷֣�)������![]() ��(1
��(1
������
����������(1��)����(1��)������(1��)������
��0.025��(2��)�����ݣ�1185KJ��mol��1
��(2��)����(3)SO2��Br2��2H2O��4H+��2Br����SO42����(2
��)
 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д� ��ѧ�����ϵ�д�
��ѧ�����ϵ�д�