题目内容
15.2015年10月,中国科学家屠呦呦因为创制了新型抗疟药--青蒿素,获得诺贝尔生理学或医学奖.青蒿素可由香茅醛为原料制取,下列说法不正确的是( ) →
→
| A. | 香茅醛能使Br2的CCl4溶液褪色 | |
| B. | 青蒿素分子中含有酯基和醚键等官能团 | |
| C. | 青蒿素在一定条件下可发生水解反应 | |
| D. | 二者均可与氢气发生加成反应 |
分析 A.香茅醛中含有碳碳双键和醛基,能和溴发生加成反应、氧化反应;
B.根据结构简式确定官能团;
C.青蒿素中含有酯基、醚键和过氧基团,具有酯、醚和过氧化物性质;
D.碳碳双键、醛基能和氢气发生加成反应,羧基和酯基不能发生加成反应.
解答 解:A.香茅醛中含有碳碳双键和醛基,能和溴发生加成反应、氧化反应而使溴水褪色,故A正确;
B.由结构简式可知青蒿素分子中含有酯基和醚键等官能团,故B正确;
C.青蒿素中含有酯基、醚键和过氧基团,具有酯、醚和过氧化物性质,酯基在一定条件下能发生水解反应,故C正确;
D.碳碳双键、醛基能和氢气发生加成反应,羧基和酯基不能发生加成反应,所以香茅醛能发生加成反应,青蒿素不能发生加成反应,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃、醛、酯的性质,注意:酯基和羧基不能发生加成反应,但羰基和醛基能发生加成反应.

练习册系列答案
相关题目
10.下列用洗净的废铜屑制备硝酸铜的方案中,能节约原料和防止环境污染的是( )
| A. | Cu+HNO3(浓)→Cu(NO3)2 | |
| B. | Cu+HNO3(稀)→Cu(NO3)2 | |
| C. | Cu$→_{加热}^{空气}$CuO$\stackrel{HNO_{3}}{→}$Cu(NO3)2 | |
| D. | Cu$→_{加热}^{浓硫酸}$CuSO4$\stackrel{Ba(NO_{3})_{2}}{→}$Cu(NO3)2 |
6.CO2的转换在生产、生活中具有重要的应用.
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”.
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为HCO3-、CO32-.
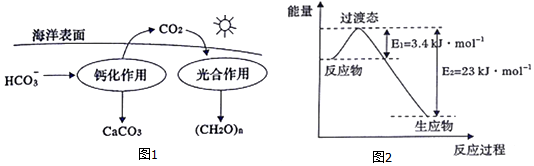
②在海洋碳循环中,可通过图1所示的途径固碳.写出钙化作用的离子方程式:Ca2++2HCO3-═CaCO3↓+CO2↑+H2O.
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 $?_{放电}^{放电}$2Na2CO3+C.放电时,在正极得电子的物质为CO2;充电时,阳极的反应式为C-4e-+2CO32-═3CO2.
(3)目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气.图2表示恒压容器中0.5molCO2和1.5mol H2转化率达80%时的能量变化示意图.能判断该反应达到化学平衡状态的依据B、D(填字母).
A.容器中压强不变 B.H2的体积分数不变
C.c(H2=3c(CH3OH) D.容器中密度不变
E.2个C=O断裂的同时有6个H-H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
①实验2条件下平衡常数K=$\frac{1}{6}$.
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值<1 (填具体值或取值范围).
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正<v(逆)(填“<”、“>”或“=“).
(5)已知在常温常压下:
①2CH3OH(I)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(I)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-442.8kJ/mol.
(1)CO2的低碳转型对抵御气候变化具有重要意义,海洋是地球上碳元素最大的“吸收池”.
①溶于海水中的CO2主要以四种无机碳形式存在,除CO2、H2CO3两种分子外,还有两种离子的化学式为HCO3-、CO32-.
②在海洋碳循环中,可通过图1所示的途径固碳.写出钙化作用的离子方程式:Ca2++2HCO3-═CaCO3↓+CO2↑+H2O.
(2)将CO2与金属钠组合设计成Na-CO2电池,很容易实现可逆的充、放电反应,该电池反应为4Na+3CO2 $?_{放电}^{放电}$2Na2CO3+C.放电时,在正极得电子的物质为CO2;充电时,阳极的反应式为C-4e-+2CO32-═3CO2.
(3)目前工业上有一种方法是用CO2和H2在230℃并有催化剂条件下转化生成甲醇蒸汽和水蒸气.图2表示恒压容器中0.5molCO2和1.5mol H2转化率达80%时的能量变化示意图.能判断该反应达到化学平衡状态的依据B、D(填字母).

A.容器中压强不变 B.H2的体积分数不变
C.c(H2=3c(CH3OH) D.容器中密度不变
E.2个C=O断裂的同时有6个H-H断裂
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b的值<1 (填具体值或取值范围).
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时v(正<v(逆)(填“<”、“>”或“=“).
(5)已知在常温常压下:
①2CH3OH(I)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(I)△H=-44.0kJ•mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式CH3OH(l)+O2(g)═CO(g)+2H2O(l)△H=-442.8kJ/mol.
3.通常情况下能共存且能用浓硫酸干燥的气体组是( )
| A. | SO2、Cl2、H2S | B. | O2、H2、SO2 | C. | NO、H2、O2 | D. | CO、NH3、O2 |
20.下列物质露置于干燥的空气中,不发生变化的是( )
| A. | Na2O | B. | Na2O2 | C. | NaHCO3 | D. | Na2CO3•10H2O |
4.我国古代四大发明中的黑火药为硝酸钾、硫磺和木炭的混合物,黑火药发生爆炸的反应式为:
2KNO3+S+3C$\frac{\underline{\;爆炸\;}}{\;}$K2S+N2↑+3CO2↑,下列有关叙述中正确的是( )
2KNO3+S+3C$\frac{\underline{\;爆炸\;}}{\;}$K2S+N2↑+3CO2↑,下列有关叙述中正确的是( )
| A. | 在黑火药爆炸的反应中,硝酸钾为氧化剂,硫磺和木炭为还原剂 | |
| B. | 在黑火药爆炸的反应中,当有1molKNO3反应时,转移电子的总物质的量为5mol | |
| C. | 三种反应物可以形成三种不同类型的晶体,三种生成物可以形成两种不同类型的晶体 | |
| D. | 在K2S晶体中,K+与S2-电子层结构相同,但K+半径大于S2-半径 |
 H溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是
H溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是