题目内容
4.垃圾分类并回收利用,符合可持续发展的要求,是垃圾处理的发展方向.对.(判断对错)分析 根据垃圾的分类和性质采取科学的方法处理,不能随意丢弃、掩埋或焚烧,处理垃圾应首先分类回收,最大限度减少资源的浪费.
解答 解:垃圾处理的一项有效方式是将其分类回收利用,既节约资源,又防止污染,符合可持续发展的要求,
故答案为:对.
点评 本题考查垃圾处理,题目难度不大,注意常见垃圾的类型以及正确的处理方法,学习中注意把握相关知识.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.下列四个数据是不同条件下测出的合成氨的反应的速率,其中最慢的是( )
| A. | v(NH3)=0.15 mol/L•min | B. | v(H2)=0.1 mol/L•min | ||
| C. | v(N2)=0.1 mol/L•min | D. | v(N2)=0.002 mol/L•s |
15.通过观察化学实验现象,分析归纳出正确的结论,是学习化学科学最基本的技能之一.下列由实验现象得出正确结论的是( )
| 选项 | 实验现象 | 结论 |
| A | 把相同大小的一块铝和镁分别投入相同浓度的NaOH溶液中:铝溶解有气泡放出,而镁没有任何变化 | 由此得出:铝的金属性比镁强 |
| B | 取一块铝箔,用酒精灯点燃:铝箔只熔化成液体而没有脱落 | 由此得出:铝不易燃烧 |
| C | 向氯化铵溶液中投入一铝片:铝片上产生大量气泡 | 由此得出:该气体是氨气 |
| D | 向氯化铝溶液中逐滴滴加NaOH溶液至过量:先产生白色沉淀,后沉淀逐渐溶解,最后沉淀完全消失 | 由此得出:氢氧化铝能溶于强碱溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,18gH2O中所含的质子数为10NA | |
| B. | 标准状况下,11.2LO2参加反应转移的电子数一定为2 NA | |
| C. | 28gN2和CO的混合气体中含有的分子数为NA | |
| D. | 5.6g铁与过量稀硫酸反应失去电子数为0.3 NA |
9.硼酸(H3BO3)在食品、医药领域应用广泛.在其他条件相同时,反应H3BO3+3CH3OH?B(OCH3)3+3H2O中,
H3BO3的转化率(α)在不同温度下随反应时间(t)的变化如右图,由此图可以得出:该反应的△H( )

H3BO3的转化率(α)在不同温度下随反应时间(t)的变化如右图,由此图可以得出:该反应的△H( )

| A. | △H<0 | B. | △H>0 | C. | △H=0 | D. | 无法判断 |
16.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A. | 元素A、B组成的化合物常温下不一定呈气态 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 化合物AE与CE含有相同类型的化学键 | |
| D. | 工业上常用电解法电解熔融的DE3制备元素D的单质 |
13.阿伏加德罗常数约为6.02×1023mol-1,下列叙述正确的是( )
| A. | 58.5 g的氯化钠固体中含有NA个氯化钠分子 | |
| B. | 0.1 L 3 mo1•L-1的NH4NO3溶液中含有的NH4+数目为0.3×6.02×1023 | |
| C. | 5.6 g铁粉与硝酸反应失去的电子数一定为0.3×6.02×1023 | |
| D. | 4.5 g SiO2晶体中含有的硅氧键数目为0.3×6.02×1023 |
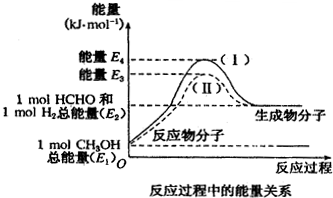
 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.