题目内容
用NA表示阿伏加德罗常数。下列说法中,正确的是
A.2.0g重水(2H2O)中含有的质子数为1.0 NA
B.0.1mol丙烯酸中含有双键的数目为0.1NA
C.标准状况下,11.2 LCl2通入足量的石灰乳中制备漂白粉,转移的电子数为NA
D.标准状况下,2.24L苯中含有的C-H键的数目为0.6NA
A
【解析】
试题分析:A、2.0g重水的物质的量是2.0g÷20g/mo=0.1mol,水中含有10个质子,则其中含有的质子数为1.0 NA,A正确;B、丙烯酸中含有1个碳碳双键和1和碳氧双键,因此0.1mol丙烯酸中含有双键的数目为0.2NA,B错误;C、标准状况下,11.2 LCl2的物质的量是0.5mol。通入足量的石灰乳中制备漂白粉,在反应中氯气既是氧化剂,也是还原剂,1分子氯气转移1个电子,则反应中转移的电子数为0.5NA,C错误;D、标准状况下苯不是气态,不能适用于气体摩尔体积,D错误,答案选A。
考点:考查阿伏伽德罗常数的计算

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
 物质成分的实验中,下列根据实验现象得出的结论正
物质成分的实验中,下列根据实验现象得出的结论正 确的是
确的是

 放电的电极反应式为________ ____。
放电的电极反应式为________ ____。 2NH3(g) △H= —39.2 KJ·mol-1
2NH3(g) △H= —39.2 KJ·mol-1  2H2O(g) △H= —486 KJ·mol-1 ,则H2 的燃烧热△H为—243 KJ·mol-1
2H2O(g) △H= —486 KJ·mol-1 ,则H2 的燃烧热△H为—243 KJ·mol-1 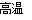 2Al2O3(s)+3Tic(s) △H=-1176kJ/mol。则反应过程中,每转移1 mol电子放出的热量为________。
2Al2O3(s)+3Tic(s) △H=-1176kJ/mol。则反应过程中,每转移1 mol电子放出的热量为________。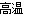 3Ba↑+BaO·Al2O3。利用化学平衡移动原理解释上述方法可制取金属Ba的原因是_____________________________________________________________________________。
3Ba↑+BaO·Al2O3。利用化学平衡移动原理解释上述方法可制取金属Ba的原因是_____________________________________________________________________________。