题目内容
透明待测溶液呈酸性,其中可能含有Na+、![]() 、Fe2+、Fe3+、Ag+、
、Fe2+、Fe3+、Ag+、![]() 、I-、
、I-、![]() 中的某些离子,现进行实验分下述3步操作:
中的某些离子,现进行实验分下述3步操作:
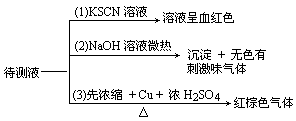
(1)推断待测液中肯定存在的离子是________
(2)肯定不存在的离子是________,判断依据是________
(3)尚不能确定溶液是否存在的离子是________
答案:
解析:
解析:
|
(1) (2)I-、Fe2+,酸性溶液中 (3)Na+,Ag+,或Na+, |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目


