题目内容
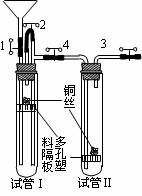
某教师用如下图所示装置做“稀硝酸的氧化性及NO的性质等”演示实验。图中1、2、3、4为止水夹。操作步骤如下:
①检查装置的气密性;
②打开1、2、3、4,经漏斗加入稀硝酸,直至酸液充满试管I;
③关闭1、2,打开3、4,用酒精灯微热试管I,当铜丝表面有气泡产生时,立即撤去酒精灯;
④随着反应进行,I中液体会流入II并浸没隔板上的铜丝,此时立即加热试管II,即可看到II中有红棕色气体产生。当红棕色气体充满II后,立即关闭3;
⑤一段时间后,关闭4并撤去酒精灯,将试管II(连同塞子及止水夹3、4)浸入盛有冰水的大烧杯中。
试回答下列问题:
(1)步骤②中稀硝酸要充满试管I的目的是_______________________________ 。
(2)步骤③中发生反应的离子方程式为_________________________________________。
(3)步骤④中产生红棕色气体的化学方程式是_________________________________。
该步骤中关闭3产生的结果是___________________________________________。
(4)实验中观察到初始阶段步骤④中产生气体的速率明显快于步骤③,你认为其可能的原因是_____________________________________________。(写出一条即可)
(5)步骤⑤中可观察到的主要现象是_________________________________________。
(1)排尽试管I中的空气,防止产生的气体被氧化
(2)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(3)2NO+O2=2NO2 会使稀硝酸重新回流到试管I中,脱离铜丝
(4)可能是反应生成的Cu2+起催化作用;可能是溶液中溶解的少量NO起催化作用;溶液的温度比较高(只要言之有理、自圆其说即给分)
(5)试管内气体的红棕色变浅

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案

