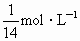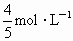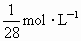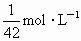题目内容
在标准状况下,将![]() 和
和![]() 的混合气,缓慢通过足量
的混合气,缓慢通过足量![]() 并充分反应,通入倒扣在水中充有17.92mLNO的量筒中,反应完毕,量筒内剩余气体体积为0.56mL.计算原混合气的可能组成.
并充分反应,通入倒扣在水中充有17.92mLNO的量筒中,反应完毕,量筒内剩余气体体积为0.56mL.计算原混合气的可能组成.
答案:
解析:
提示:
解析:
|
答案: (1)当氧气过量时,
(2)当氧气不足时,
把
在这一反应中2体积 氧气与一氧化氮混合并被水吸收时,发生的化学反应方程式为:
把②③两个化学反应方程式可以合并写为:
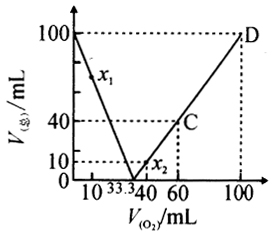
从反应方程式⑤可以看出,当NO与 解法(1)当氧气过量时,剩余0.56mL尾气是氧气.设跟17.92mLNO反应的适量氧气的体积为xmL.
设在15.68mL混合气中的二氧化碳体积为
(2)当氧气不足时,反应后剩余尾气是0.56mL一氧化氮.设跟17.92mLNO混合的
设在15.68mL混合气中的二氧化碳体积为
|
提示:
|
本题要运用逆向思维先算出跟17.92mL一氧化氮混合的氧气体积;然后,利用体积差算出混合气的组成;要善于利用关系式,使计算简化;善于思维发散,算出两组不同的解.这是这道算题解题的三个要点. |

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
 和
和 按1∶4体积比充满一干燥的烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,最后烧瓶内溶液的物质的量浓度是
按1∶4体积比充满一干燥的烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,最后烧瓶内溶液的物质的量浓度是 和
和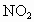 按1∶4的体积比充满干燥烧瓶,把烧瓶倒置于水中,瓶内液体逐渐上升,假设烧瓶内溶液不散,最终烧瓶内溶液里溶质的物质的量浓度为
按1∶4的体积比充满干燥烧瓶,把烧瓶倒置于水中,瓶内液体逐渐上升,假设烧瓶内溶液不散,最终烧瓶内溶液里溶质的物质的量浓度为