题目内容
由金红石(TiO2)制取单质Ti,涉及到的部分步骤为
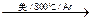 Ti
Ti
已知:①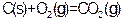
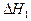 ②
②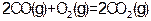
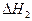
③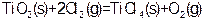

则反应 的
的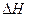 为
为

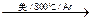 Ti
Ti已知:①
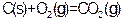
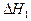 ②
②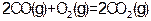
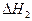
③
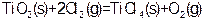

则反应
 的
的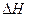 为
为A. +2 +2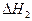 -2 -2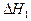 | B. +2 +2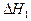 + +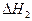 |
C. +2 +2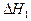 - -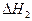 | D. +2 +2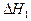 -2 -2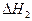 |
C
略

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
题目内容

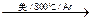 Ti
Ti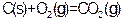
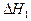 ②
②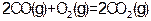
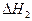
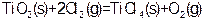

 的
的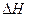 为
为A. +2 +2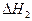 -2 -2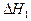 | B. +2 +2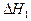 + +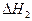 |
C. +2 +2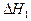 - -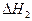 | D. +2 +2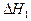 -2 -2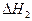 |

 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案