题目内容
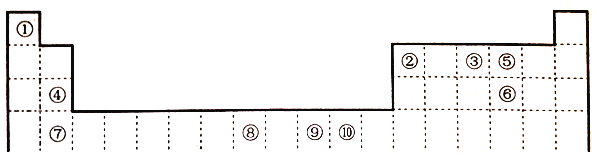
【题目】下列装置或操作能达到实验目的的是

A.①②B.③④C.②③④D.①②③④
【答案】B
【解析】
①从碘水中分离碘单质,应该使用萃取的方法,并选用CCl4或苯作萃取剂,故①错误;
②铜与稀硝酸反应生成NO,NO与空气中的氧气反应生成NO2,且NO与空气密度相差较小,所以不能用排空气法收集NO,故②错误;
③铁生锈要有空气和一定的湿度才行,在水里和盐溶液里面除了满足上述两个条件以外,还有加速铁生锈的另一个重要因素电解质,由于电解质的存在会大大加快生锈的速度,含量越高就越快,食盐水是电解质,电解质加速铁生锈的速度,根据右面红墨水液面的变化可证明铁生锈空气参与反应,能达到目的,故③正确;
④检查装置气密性可以采取“注水法”:首先关闭排气导管,从顶部漏斗口注水,当漏斗下端被水封闭后再注水,水面不下降,表明装置气密性好;如果水面下降,表明装置气密性差,能达到目的,故④正确;
能达到实验目的的是③④,答案选B。

练习册系列答案
相关题目
【题目】25 ℃下,部分弱酸的电离常数如表。下列有关说法正确的是
弱酸 | HCOOH | HClO | H2S |
电离平衡 常数(Ka) | Ka=1.0×10-4 | Ka=2.0×10-8 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
A.相同浓度的HCOOH和HClO溶液的pH后者小
B.若HCOONa和HCOOH的混合溶液的pH=3,则![]() =10
=10
C.任何浓度NaHS溶液中总存在:c(Na+)+c(H+)=c(OH-)+c(HS-)
D.向NaClO溶液中通入H2S发生的反应为2ClO-+H2S===S2-+2HClO