题目内容
在通常状况下37.0g由气态烷烃组成的混合物完全燃烧消耗4.25mol O2,此混合物可能组合的方式最多有
- A.3种
- B.4种
- C.5种
- D.6种
D
分析:设该混合烃的平均分子式为CxHy,根据方程式CxHy +(x+ )O2
)O2  xCO2+
xCO2+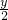 H2O结合烃的质量、氧气的物质的量列出有关x、y的方程,求出x、y的关系,结合通常条件下为气体,进行讨论.
H2O结合烃的质量、氧气的物质的量列出有关x、y的方程,求出x、y的关系,结合通常条件下为气体,进行讨论.
解答:设该混合烃的平均分子式为CxHy,则
由:CxHy +(x+ )O2
)O2  xCO2+
xCO2+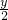 H2O得下列方程:
H2O得下列方程:
(12x+y)g (x+ )mol
)mol
37g 4.25mol
所以(12x+y):37=(x+ ):4.25,解得y:x=2.8:1,即分子式中n(H):n(C)=2.8,
):4.25,解得y:x=2.8:1,即分子式中n(H):n(C)=2.8,
而CH4分子中n(H):n(C)=4,C2H6中n(H):n(C)=3,C3H8中n(H):n(C)=2.67,C4H10中n(H):n(C)=2.5,而C4H10有2种同分异构体,故符合题意的组合有:①CH4和C3H8 ②CH4和正丁烷 ③CH4和异丁烷 ④C2H6和C3H8 ⑤C2H6和正丁烷 ⑥C2H6和异丁烷共6种.
故选:D.
点评:考查烃混合物分子式确定,难度较大,注意利用平均分子组成判断烃的组成,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.本题也可以令平均分子式为CxH2x+2,求平均分子式.
分析:设该混合烃的平均分子式为CxHy,根据方程式CxHy +(x+
 )O2
)O2  xCO2+
xCO2+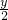 H2O结合烃的质量、氧气的物质的量列出有关x、y的方程,求出x、y的关系,结合通常条件下为气体,进行讨论.
H2O结合烃的质量、氧气的物质的量列出有关x、y的方程,求出x、y的关系,结合通常条件下为气体,进行讨论.解答:设该混合烃的平均分子式为CxHy,则
由:CxHy +(x+
 )O2
)O2  xCO2+
xCO2+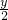 H2O得下列方程:
H2O得下列方程:(12x+y)g (x+
 )mol
)mol37g 4.25mol
所以(12x+y):37=(x+
 ):4.25,解得y:x=2.8:1,即分子式中n(H):n(C)=2.8,
):4.25,解得y:x=2.8:1,即分子式中n(H):n(C)=2.8,而CH4分子中n(H):n(C)=4,C2H6中n(H):n(C)=3,C3H8中n(H):n(C)=2.67,C4H10中n(H):n(C)=2.5,而C4H10有2种同分异构体,故符合题意的组合有:①CH4和C3H8 ②CH4和正丁烷 ③CH4和异丁烷 ④C2H6和C3H8 ⑤C2H6和正丁烷 ⑥C2H6和异丁烷共6种.
故选:D.
点评:考查烃混合物分子式确定,难度较大,注意利用平均分子组成判断烃的组成,常用方法有1、平均碳法 2、平均氢法 3、平均碳氢分子式法 4、平均式量法.本题也可以令平均分子式为CxH2x+2,求平均分子式.

练习册系列答案
相关题目