��Ŀ����
300��ʱ����2 mol A��2 mol B������������2 L�ܱ������У��������·�Ӧ��
3A(g)��B(g)  2C(g)��2D(g)����H��Q��2 minĩ�ﵽƽ�⣬����0.8 mol D.
2C(g)��2D(g)����H��Q��2 minĩ�ﵽƽ�⣬����0.8 mol D.
(1)300��ʱ���÷�Ӧ��ƽ�ⳣ������ʽΪ��K��___________.
��֪K300��<K350������H________0(���������)��
(2)��2 minĩʱ��B��ƽ��Ũ��Ϊ________��D��ƽ����Ӧ����Ϊ______________��
(3)���¶Ȳ��䣬��С�����ݻ�����A��ת����________(���������С�����䡱)��ԭ����__________________________________________________��
(4)�������ͬ�������£�������Ӧ���淴Ӧ������У���ʼʱ������C��D��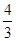 mol.��ʹƽ��ʱ�����ʵ����ʵ���Ũ����ԭƽ����ͬ����Ӧ�ü���B________ mol.
mol.��ʹƽ��ʱ�����ʵ����ʵ���Ũ����ԭƽ����ͬ����Ӧ�ü���B________ mol.
����10��,ǰ4��ÿ�ո�1�֣�����ÿ��2�֣�
(1)K��c2(C)��c2(D)/ c3(A) ��c (B) ����
(2) 0.8 mol��L��1 0��2 mol��L��1��min��1
(3)���䡡 ��Ӧǰ������������䣬ѹǿ��ƽ����Ӱ�졡(4) 
��������
���������(1) ��ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ�Ӧ�Ļ�ѧ����ʽ��֪��300��ʱ���÷�Ӧ��ƽ�ⳣ������ʽΪK��c2(C)��c2(D)/ c3(A) ��c (B)�����K300��<K350������˵�������¶ȣ�ƽ��������Ӧ�����ƶ�����H��0��
��2��
3A(g)��B(g)  2C(g)��2D(g)
2C(g)��2D(g)
��ʼŨ�ȣ�mol/L�� 1 1 0 0
ת��Ũ�ȣ�mol/L�� 0.6 0.2 0.4 0.4
ƽ��Ũ�ȣ�mol/L�� 0.4 0.8 0.4 0.4
����D��ƽ����Ӧ����Ϊ0.4mol/L��2min��0��2 mol��L��1��min��1
��3����Ӧǰ������������䣬ѹǿ��ƽ����Ӱ�죬�������¶Ȳ��䣬��С�����ݻ�����A��ת���ʲ��䡣
��4���������ͬ�������£�������Ӧ���淴Ӧ������У����C��D����ת��ΪA��B֮��Ӧ�ú����A��B�����ʵ�����ȡ�C��D�� mol��ȫת��ΪA��2mol��B��
mol��ȫת��ΪA��2mol��B�� �����Ի�Ӧ�ü���B��2mol��
�����Ի�Ӧ�ü���B��2mol�� ��
�� ��
��
���㣺����ƽ�ⳣ����Ӧ�á���Ӧ�����Լ���Чƽ����йؼ���
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������͡����������ǿ���������С���ע�ض�ѧ��������֪ʶ���̺�ѵ����ͬʱ�����ض�ѧ�����ⷽ��������������������������ѧ�������������������ѧ����Ӧ��������������ѵ��ǵ�Чƽ����жϺ��йؼ��㡣

 һ����ʦȨ����ҵ��ϵ�д�
һ����ʦȨ����ҵ��ϵ�д�
| c(X)/ mol��L-1 | c(Y)/ mol��L-1 | v/ mol��L-1��s-1 |
1 | 0.10 | 0.10 | 4.0��10-4 |
2 | 0.20 | 0.10 | 1.6��10-3 |
3 | 0.30 | 0.10 | 3.6��10-3 |
4 | 0.30 | 0.20 | 7.2��10-3 |
��������ʵ�����ݣ�����������⣺
��1��������Ӧ��
��2����c(X)=c(Y)=0.25 mol��L-1ʱ��v=_______________��
��8�֣���ͭ�����Ҫ�ɷ�X����Cu��Fe��S����Ԫ����ɵĸ��Σ�����Cu��Fe����Ԫ�ص�������Ϊ8��7����m g X��ĩȫ������200 mL��ŨHNO3����Ӧ�����Һ��ˮϡ�� 2.12 Lʱ�����pH��0����ϡ�ͺ����Һ��Ϊ���ȷݣ�������һ����Һ�еμ�Ũ��Ϊ6. 05 mol/L��NaOH��Һ������һ����Һ�еμ�0.600 mol/L Ba(NO3)2��Һ������Һ�о����ɳ������ҳ�����������������Һ������仯����ͼ��ʾ��
��1����ͨ������ȷ����m��________��
��2��X��Ħ������Ϊ368 g/mol����X�Ļ�ѧʽΪ________________��
��3����һ��������Fe��Cu�Ļ����ƽ���ֳ��ĵȷݣ�ÿ��13.2 g���ֱ����ͬŨ�ȵ�ϡ���ᣬ��ַ�Ӧ���ڱ�״��������NO�������ʣ��������������±���������Ļ�ԭ����ֻ��NO����
| ʵ���� | �� | �� | �� | �� |
| ϡ�������/mL | 100 | 200 | 300 | 400 |
| ʣ���������/g | 9.0 | 4.8 | 0 | 0 |
| NO���/L | 1.12 | 2.24 | 3.36 | V |
�ش��������⣺
��д��ʵ����з�����Ӧ�����ӷ���ʽ___________________________________��
��ʵ�����V��________��