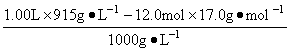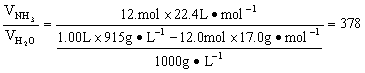题目内容
标准状况下,用一定量的水吸收氨气后制得浓度为12.0mol·L-1、密度为0.915g·cm-3的氨水。试计算1体积水吸收多少体积的氨气可制得上述氨水。 (本题中氨的式量以17.0计,水的密度以1.00g·cm-3计)
答案:
解析:
提示:
解析:
| 1.00L该氨水中含氨的质量为:12.0mol×17.0g·mol-1
其体积在标准状况下为:12.0mol×22.4L·mol-1 1.00L该氨水中含水的质量为: 1.00L×915g·L-1-12.0mol× 17.0g·mol-1 其体积为:
|
提示:
| 已知1L氨水中溶有12.0molNH3,即氨水中含17.0g·mol-1×12.0mol=204g的NH3.这些NH3在标准状况下应该是12.0mol×22.4L·mol-1=268.8L.如果氨水的密度是0.915g·cm-3,则1L氨水中实有的水的质量应该是0.915g·cm-3.×1000cm3-204g=711g.题目要求1体积水吸收的氨气的体积,水的密度以1.00g·cm-3计,则将氨气体积除以水的体积即得
|

练习册系列答案
相关题目