题目内容
【化学与技术】
工业上制取铝的流程如下:
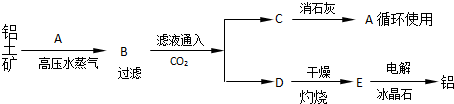
注:冰晶石的作用是使E在较低温度下熔化.
(1)试写出下列物质的化学式:A ,B ,C ,D ,E .
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
试求制取1t Al2O3所需铝土矿和苛性钠的质量.(写过程)
工业上制取铝的流程如下:

注:冰晶石的作用是使E在较低温度下熔化.
(1)试写出下列物质的化学式:A
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| Al2O3 | Fe2O3 | Na2O | |
| 铝土矿 | 55% | 16% | 0% |
| 赤泥 | 15% | 48% | 8% |
分析:(1)铝土矿的成分中,只有氧化铝可以和氢氧化钠之间发生反应生成偏铝酸钠溶液,向其中通入二氧化碳会生成氢氧化铝和碳酸钠溶液,氢氧化铝易分解为氧化铝和水,电解熔融的氧化铝可以得到金属铝和氧气,所以A是氢氧化钠,B是二氧化碳,C是碳酸钠或是碳酸氢钠,D是氢氧化铝,E是氧化铝;
(2)根据元素守恒结合物质的质量进行计算即可.
(2)根据元素守恒结合物质的质量进行计算即可.
解答:解:(1)铝土矿的成分中,只有氧化铝可以和氢氧化钠之间发生反应生成偏铝酸钠溶液,向其中通入二氧化碳会生成氢氧化铝和碳酸钠溶液,氢氧化铝易分解为氧化铝和水,电解熔融的氧化铝可以得到金属铝和氧气,所以A是氢氧化钠,B是二氧化碳,C是碳酸钠或是碳酸氢钠,D是氢氧化铝,E是氧化铝,
故答案为:NaOH;NaAlO2;NaHCO3或Na2CO3;Al(OH)3;Al2O3;
(2)铝土矿中,氧化铝的质量分数是55%,所以1tAl2O3所需铝土矿的质量m=
≈1.8t,氧化铝和氢氧化钠之间的反应:Al2O3+2NaOH=2NaAlO2+H2O,所以1tAl2O3所需氢氧化钠的质量m=0.78t,
答:铝土矿中,氧化铝的质量分数是55%,所以1tAl2O3所需铝土矿的质量m=
≈1.8t,氧化铝和氢氧化钠之间的反应:Al2O3+2NaOH=2NaAlO2+H2O,所以1tAl2O3所需氢氧化钠的质量m=0.78t.
故答案为:NaOH;NaAlO2;NaHCO3或Na2CO3;Al(OH)3;Al2O3;
(2)铝土矿中,氧化铝的质量分数是55%,所以1tAl2O3所需铝土矿的质量m=
| 1t |
| 55% |
答:铝土矿中,氧化铝的质量分数是55%,所以1tAl2O3所需铝土矿的质量m=
| 1t |
| 55% |
点评:本题考查学生金属铝以及化合物的性质知识,注意知识的归纳和整理是解题关键,难度不大.

练习册系列答案
相关题目



 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是__________________、__________________。
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是__________________、__________________。  7N2+12H2O(NO 也有类似的反应)
7N2+12H2O(NO 也有类似的反应)