题目内容
某学生用一定溶质质量分数的稀硫酸和氧化铜进行反应,实验结果如下所示:
|
实验次数m |
(CuO)/g |
硫酸溶液/mL |
m(CuSO4)/g |
|
一 |
2.0 |
120 |
4.0 |
|
二 |
4.0 |
120 |
8.0 |
|
三 |
6.0 |
120 |
9.6 |
|
四 |
8.0 |
200 |
16.0 |
|
五 |
10.0 |
200 |
x |
根据实验结果填写下列空格:
(1)哪几次反应硫酸有剩余?________.
(2)哪几次反应氧化铜有剩余?________.
(3)上面的x值是多少?________.
答案:
解析:
解析:
|
(1)一,二;(2)三,五;(3)16.0 导解:观察各次实验数据知:在一、二、三次中、V(H2SO4)保持120mL不变,而m(CuSO4)逐渐增加,知在第一,二次实验中,H2SO4有剩余,CuO消耗完,生成CuSO4质量与消耗CuO质量之比α1= |

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
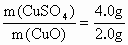 =2,对第二次实验,若CuO消耗完,则m(CuSO4)=α1·m(CuO)=2×6.0g=12g,而m(CuSO4)实际上为9.6g,知CuO有剩余,H2SO4消耗完,生成CuSO4质量与消耗H2SO4体积之比α2=
=2,对第二次实验,若CuO消耗完,则m(CuSO4)=α1·m(CuO)=2×6.0g=12g,而m(CuSO4)实际上为9.6g,知CuO有剩余,H2SO4消耗完,生成CuSO4质量与消耗H2SO4体积之比α2=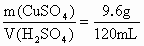 ,对第四次,验证可知m(CuSO4)=m(CuO)·α1=V(H2SO4)·α2,即CuO和H2SO4恰好完全反应,故对第五次,可知CuO有剩余,此时生成CuSO4质量x应仍为16.0g.
,对第四次,验证可知m(CuSO4)=m(CuO)·α1=V(H2SO4)·α2,即CuO和H2SO4恰好完全反应,故对第五次,可知CuO有剩余,此时生成CuSO4质量x应仍为16.0g.

