题目内容
CH2Br-CH2Br 的命名为1,2--二溴乙烷. .(判断对错说明理由)
考点:有机化合物命名
专题:有机物分子组成通式的应用规律
分析:该有机物分子中含有2个溴原子,为乙烷的二溴取代产物,命名时需要指出官能团所处的位置及数目,据此对该有机物的命名进行判断.
解答:
解:CH2Br-CH2Br,该有机物中含有官能团溴原子,相当于两个溴原子分别取代了乙烷中两个C原子的1个H形成的,该有机物名称为:1,2-二溴乙烷,所以该命名是正确的,
故答案为:√,符合有机物的命名原则.
故答案为:√,符合有机物的命名原则.
点评:本题考查了有机物的命名的判断,题目难度不大,该题注重了基础性试题的考查,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
某化学反应2M+N→3F是一步完成的,M和N的起始浓度分别为2mol/L和4mol/L,1秒钟后,M的浓度下降了1mol/L,下面结论中正确的是( )
| A、F的浓度为1.5mol/L |
| B、F的浓度为1mol/L |
| C、N的浓度为2.5mol/L |
| D、N的浓度为3mol/L |
下列化合物中阳离子半径与阴离子半径比值最大的是( )
| A、NaF |
| B、LiI |
| C、MgI2 |
| D、KF |
 (Ⅰ)已知:H+(aq)+OH-(aq)═H2O(l)△H1=-57.3kJ/mol
(Ⅰ)已知:H+(aq)+OH-(aq)═H2O(l)△H1=-57.3kJ/mol 工业上常用天然气作为制备甲醇CH3OH的原料.已知:
工业上常用天然气作为制备甲醇CH3OH的原料.已知:
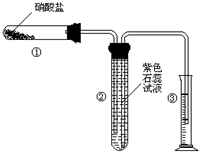 某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)
某校化学兴趣小组的同学对硝酸盐的受热分解进行探究.他们设计了如下装置分别加热了Ca(NO3)2、Cu(NO3)2、AgNO3三种固体.(加热及夹持装置未画出)