题目内容
下列图示与对应的叙述相符的是( )
A、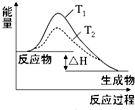 表示SO2与O2反应过程中的能量变化,其中T1>T2 | B、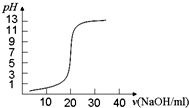 表示0.1000mol?L-1 NaOH溶液滴定20.00ml 0.1000mol?L-1 CH3COOH溶液所得到的滴定曲线 | C、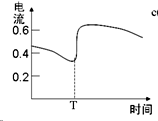 表示酸性介质Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2 | D、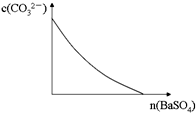 表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 |
分析:A、图象分析两个途径变化过程不同,反应物和生成物的能量相同,反应过程中的能量变化相同,T1和T2比较是同温下加入催化剂发生的改变;
B、0.1000mol?L-1 NaOH溶液滴定20.00ml 0.1000mol?L-1 CH3COOH溶液恰好反应需要氢氧化钠溶液体积0.00ml,生成的醋酸钠溶液成碱性;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大;
D、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0.
B、0.1000mol?L-1 NaOH溶液滴定20.00ml 0.1000mol?L-1 CH3COOH溶液恰好反应需要氢氧化钠溶液体积0.00ml,生成的醋酸钠溶液成碱性;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大;
D、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0.
解答:解:A、反应物和生成物的能量相同,图象分析两个途径变化过程不同,反应过程中的能量变化相同,T1和T2比较是同温下加入催化剂发生的改变,故A错误;
B、0.1000mol?L-1 NaOH溶液滴定20.00ml 0.1000mol?L-1 CH3COOH溶液恰好反应需要氢氧化钠溶液体积0.00ml,生成的醋酸钠溶液成碱性,图象中PH变化不符合反应过程,故B错误;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大,故C正确;
D、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0,故D错误;
故选C.
B、0.1000mol?L-1 NaOH溶液滴定20.00ml 0.1000mol?L-1 CH3COOH溶液恰好反应需要氢氧化钠溶液体积0.00ml,生成的醋酸钠溶液成碱性,图象中PH变化不符合反应过程,故B错误;
C、Zn、Cu和稀硫酸构成的原电池在工作过程中,锌失电子发生氧化反应,随稀硫酸浓度减小反应进行,电流强度减小,T时加入了H2O2,是强氧化剂,可以加快锌溶解的反应,电流强度增大,随反应进行电流强度又减小,但比开始电流强度大,故C正确;
D、饱和Na2CO3溶液中逐步加BaSO4固体后实现沉淀转化,碳酸钙离子浓度减小,但是建立的沉淀溶解和沉淀转化平衡状态,碳酸根离子不能减小为0,故D错误;
故选C.
点评:本题考查了反应过程中能量变化、酸碱反应的图象分析判断,沉淀转化关系分析,原电池原来的应用理解,题目难度中等.

练习册系列答案
相关题目
下列图示与对应的叙述一定正确的是( )
A、图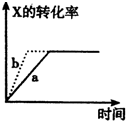 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 所示,反应:X(g)+2Y(g)?3Z(g),b的压强一定比a大 | B、图 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 | C、图 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 所示,t1℃时质量分数均为20%的甲乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 | D、图 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a 所示,用水稀释PH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |


