题目内容
19.在容积为2L的容器内,发生反应2A(s)+3B(g)?2C(g)+D(g),△H<0起始时充入3molA和2.5molB混合气体,经过5min生成0.5molD,下列说法正确的是( )| A. | B的平均消耗速率为0.3mol/(L•min) | |
| B. | 升高温度时,v正减小,v逆增大 | |
| C. | 若单位时间内生成的B和D的物质的量之比为3:1,则体系处于平衡状态 | |
| D. | 平衡后,增大压强,平衡将向正方向移动 |
分析 A.根据B的反应的量求出浓度变化,再根据速率公式计算;
B.升高温度,正逆反应速率都增大;
C.若单位时间内生成的B和D的物质的量之比为3:1,说明正逆反应速率相等;
D.增大压强,平衡向气体体积减小的方向移动.
解答 解:A.经过5min生成0.5molD,则消耗1.5molB,则B的速率为$\frac{\frac{1.5mol}{2L}}{5min}$=0.15mol/(L•min),故A错误;
B.升高温度,正逆反应速率都增大,故B错误;
C.生成B为逆反应速率,生成D为正反应速率,当二者的比值等于计量数之比即是平衡状态,故C正确;
D.反应前后气体的体积不变,增大压强,平衡不移动,故D错误.
故选C.
点评 本题考查了化学平衡的基本计算方法,为高频考点,侧重于学生的分析、计算能力的考查,注意把握速率计算的应用,平衡状态的判断,影响平衡的因素,题目难度中等.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
20.下列各组离子中,能在溶液中大量共存的是( )
| A. | H+、Ca2+、Cl-、CO32- | B. | Cl-、ClO-、K+、H+ | ||
| C. | Na+、Fe3+、SO42-、OH- | D. | Na+、Cu2+、Cl-、SO42- |
7.可用如图装置制取(必要时可加热)和收集的气体是( )
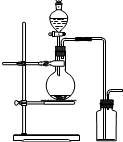

| A. | 氯酸钾溶液与二氧化锰反应制氧气 | B. | 浓氨水与氢氧化钙固体制氨气 | ||
| C. | 乙醇和浓硫酸(170℃)制乙烯 | D. | 铜和浓硝酸制二氧化氮 |
4.下列现象或事实不能用同一原理解释的是( )
| A. | 浓硝酸和氯水用棕色试剂瓶保存 | |
| B. | 硫化钠和硫酸亚铁固体长期暴露在空气中变质 | |
| C. | 常温下铁和铂都不溶于浓硝酸 | |
| D. | H2O2溶液中加入少量MnO2或FeCl3溶液都能增大反应速率 |
11.下列实验操作不正确或不能达到目的是( )
| A. | 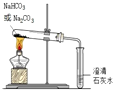 鉴别碳酸钠和碳酸氢钠 | |
| B. | 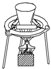 钠的燃烧 | |
| C. | 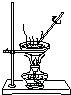 直接蒸发氯化铁溶液获得氯化铁晶体 | |
| D. | 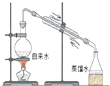 实验室制取蒸馏水 |
9.下列说法正确的是( )
| A. | 0.5molO3与11.2LO2所含的分子数一定相等 | |
| B. | 25℃与60℃时,水的pH相等 | |
| C. | 中和等体积、等物质的量的浓度的盐酸和醋酸所消耗的n(NaOH)相等 | |
| D. | 2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的△H相等 |

 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$ +CO2↑
+CO2↑ $→_{△}^{NaOH(aq)}$
$→_{△}^{NaOH(aq)}$ +H2O
+H2O $→_{(Ⅱ)H+}^{(Ⅰ)_{10}%NaOH;Cu}$
$→_{(Ⅱ)H+}^{(Ⅰ)_{10}%NaOH;Cu}$
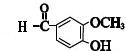 +CH3COCH2COCH3$→_{△}^{NaOH(aq)}$
+CH3COCH2COCH3$→_{△}^{NaOH(aq)}$ +2H2O.
+2H2O.
 .
.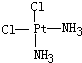 、
、 .
.