题目内容
一定温度下,在容积可变的密闭容器中发生反应CO(g)+H2O(g)=CO2(g)+H2(g)△H<0,则下列说法不正确的是( )
| A、其他条件不变,加催化剂与不加催化剂其△H相同 |
| B、当达到平衡,向体系中充入CO2其平衡向左移动 |
| C、理论上该反应可设计成燃料电池,H2O(g)在正极上发生还原反应 |
| D、平衡混合气体通入NaOH溶液恰好反应,升高温度溶液碱性增强,其pH一定增大 |
考点:化学平衡的影响因素
专题:
分析:A、焓变的大小决定于反应物和生成物能量差,与是否使用催化剂无关;
B、充入二氧化碳,生成物浓度大于反应物,平衡逆向移动;
C、原电池正极发生还原反应;
D、混合气体通入NaOH溶液恰好反应,生成碳酸钠或碳酸氢钠溶液,其水解使溶液显碱性.
B、充入二氧化碳,生成物浓度大于反应物,平衡逆向移动;
C、原电池正极发生还原反应;
D、混合气体通入NaOH溶液恰好反应,生成碳酸钠或碳酸氢钠溶液,其水解使溶液显碱性.
解答:
解:A、有无催化剂不影响焓变大小,故A正确;
B、生成物浓度增大平衡逆向移动,故B正确;
C、燃料电池中正极反应还原反应,故C错误;
D、混合气体通入NaOH溶液恰好反应,生成碳酸钠或碳酸氢钠溶液,其水解使溶液显碱性,升温能够促进盐类水解,溶液减小增强,pH增大,故D正确;
故选C.
B、生成物浓度增大平衡逆向移动,故B正确;
C、燃料电池中正极反应还原反应,故C错误;
D、混合气体通入NaOH溶液恰好反应,生成碳酸钠或碳酸氢钠溶液,其水解使溶液显碱性,升温能够促进盐类水解,溶液减小增强,pH增大,故D正确;
故选C.
点评:本题考查了焓变大小的影响因素、平衡移动、原电池的电极反应、盐类水解,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
使用一种试剂即可将酒精、苯酚溶液、己烯、甲苯4种无色液体区分开来,这种试剂是( )
| A、溴水 |
| B、金属钠 |
| C、KMnO4溶液 |
| D、FeCl3溶液 |
制取较纯的一氯乙烷,最好采用的方法是( )
| A、乙烷和氯气取代 |
| B、乙烯加成氢气,再用氯气取代 |
| C、乙烯和氯化氢加成 |
| D、乙烯和氯气加成 |
有A、B、C、D四种金属.A、B中A易失电子;将A、D分别投入等浓度盐酸中,D比A反应剧烈;将B和C用导线相联,浸入C的盐溶液里,B溶解,C上有金属C析出.据此判断它们的活动性由强到弱的顺序是( )
| A、D、C、A、B |
| B、D、A、B、C |
| C、D、B、A、C |
| D、B、A、D、C |
在一个固定容积的密闭容器中,可逆反应N2+3H2?2NH3达到平衡的标志是( )
| A、v(N2)正=v(NH3)逆 |
| B、单位时间内3mol H-H键断裂,同时2mol N-H键断裂 |
| C、n(N2):n(H2):(NH3)=1:3:2 |
| D、反应混合物各组分的物质的量浓度不再改变 |
科学家根据元素周期律和原子结构理论预测,原子序数为114的元素属于第七周期ⅣA族,称为类铅元素.下面关于它的原子结构和性质预测正确的是( )
| A、类铅元素原子的最外层电子数为4 |
| B、其常见价态为+2、+3、+4 |
| C、它的原子半径比铅小? |
| D、它的金属性比铅强 |
下列表示物质结构的化学用语正确的是( )
| A、乙烯的结构简式CH2CH2 |
| B、Na2O2中氧元素的化合价为-2 |
C、Cl-的结构示意图: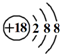 |
| D、乙烷的结构简式:CH3CH3 |

