��Ŀ����
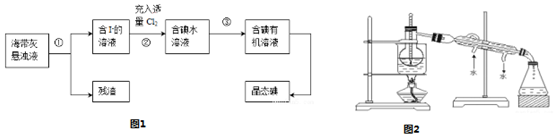
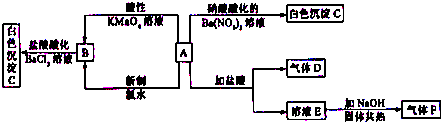
10��һ�ְ�ɫ����A��������ˮ����A�����Һ�������¿�ͼ��ʾ��ʵ�飬ʵ������ת����ϵ�����п�ͼ��ʾ������AΪ��NH4�� 2SO3������D��ʹƷ����Һ��ɫ������F��ʹʪ��ĺ�ɫʯ����ֽ�������Իش��������⣺
��1��д���������ʻ�ѧʽ��D��SO2��
��2��д�����з�Ӧ�����ӷ���ʽ��
��A������KMnO4��Һ��2MnO4-+6H++5SO32-=5SO42-+2Mn2++5H2O��
��E��NaOH��Һ��NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
��3��ͨ������Ľ���ڼ���SO42-ʱ��Ӧʹ��A-
A�������ữ��BaCl2��Һ B�������ữ��Ba��NO3��2��Һ��
���� AΪ��NH4�� 2SO3�������ᰱ�������ᷴӦ��������D��ʹƷ����Һ��ɫ���Ƕ�����������F��ʹʪ��ĺ�ɫʯ����ֽ�������ǰ�������ҺEΪ�Ȼ����Һ�����������ƹ���������ɰ����������ᰱ�����Ը��������Һ��Ӧ��Ҳ��Ϊ������B��A����ˮ��Ӧ�����Ȼ�李�������̼�ȣ���BΪ����泥����������ữ���Ȼ�����Һ�õ���ɫ����Ϊ���ᱵ�������ݴ˷����ش�
��� �⣺AΪ��NH4�� 2SO3�������ᰱ�������ᷴӦ��������D��ʹƷ����Һ��ɫ���Ƕ�����������F��ʹʪ��ĺ�ɫʯ����ֽ�������ǰ�������ҺEΪ�Ȼ����Һ�����������ƹ���������ɰ����������ᰱ�����Ը��������Һ��Ӧ��Ҳ��Ϊ������B��A����ˮ��Ӧ�����Ȼ�李�������̼�ȣ���BΪ����泥����������ữ���Ȼ�����Һ�õ���ɫ����Ϊ���ᱵ������
��1����NH4��2SO3�ܺ����ᷴӦ���ɶ�����������D��SO2��
�ʴ�Ϊ��SO2��
��2����A������KMnO4��Һ��Ӧ���ӷ���ʽΪ��2MnO4-+6H++5SO32-=5SO42-+2Mn2++5H2O���ʴ�Ϊ��2MnO4-+6H++5SO32-=5SO42-+2Mn2++5H2O��
��EΪ�Ȼ����Һ���������ƹ�����ȷ�Ӧ����κ�ǿ��Ȼ����ɰ�������һ�ּ������壬��Ӧ�����ӷ���ʽΪ��NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
�ʴ�Ϊ��NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O��
�ʴ�Ϊ��Cl2+H2O+SO32-=SO42-+2H++2Cl-��
��3���������ǿ�����ԣ����Խ�SO32-����ΪSO42-����Ӱ��SO42-�ļ��飬�ڼ���SO42-ʱ��Ӧʹ�� �����ữ��BaCl2��Һ������ȷ����Һ�в���Ag+�ȸ������Ӵ���ʱ��ѡ�������ữ��BaCl2��Һ���Լ�����SO42-����ȷ����Һ�в���SO32-�ȸ������Ӵ���ʱ��ѡ��HNO3�ữ��Ba��NO3��2��Һ���Լ�����SO42-��
�ʴ�Ϊ��A��
���� ����Ϊ����ͼ�ƶ��⣬Ϊ�߿��������ͣ����ؿ���ѧ���ķ���������ʵ��������ע��Ѱ�ҽ����ͻ�ƿ��ǹؼ�����Ҫ�������ʵ����ʣ��ѶȲ������ʱע��������ӵļ��鷽����ʵ����ƣ�

 I����NH3����ԭNxOy�������������������Ⱦ��
I����NH3����ԭNxOy�������������������Ⱦ����֪����Ӧ�٣�4NH3��g��+6NO��g��?5N2��g��+6H2O��l����H1
��Ӧ�ڣ�2NO��g��+O2��g��?2NO2��g����H2 ����|��H1|=2|��H2|��
��Ӧ�ۣ�4NH3��g��+6NO2��g��?5N2��g��+3O2��g��+6H2O��l����H3
��Ӧ�ٺͷ�Ӧ���ڲ�ͬ�¶�ʱ��ƽ�ⳣ�������С��ϵ���
| �¶�/K | ��Ӧ�� | ��Ӧ�� | ��֪�� K2��K1��K2�䣾K1�� |
| 298 | K1 | K2 | |
| 398 | K1�� | K2�� |
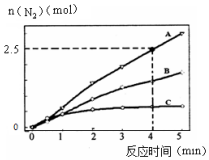
��2����ͬ�����£���Ӧ����2L�ܱ������ڣ�ѡ�ò�ͬ��������Ӧ����N2������ʱ��仯��ͼ��ʾ��
�ټ���0��4������A���������£���Ӧ����v��NO��=0.375mol•L-1•min-1��
������˵����ȷ����CD��
A���÷�Ӧ�Ļ�ܴ�С˳���ǣ�Ea��A����Ea��B����Ea��C��
B������ѹǿ��ʹ��Ӧ���ʼӿ죬����Ϊ���ӻ���Ӱٷ���
C����λʱ����H-O����N-H�����ѵ���Ŀ���ʱ��˵����Ӧ�Ѿ��ﵽƽ��
D�����ں��ݾ��ȵ��ܱ������з�����Ӧ�����¶Ȳ���ʱ��˵����Ӧ�Ѿ��ﵽƽ�⣮
| A�� | һ���¶��£�1 L 0.50 mol•L-1 NH4Cl��Һ��2 L 0.25 mol•L-1 NH4Cl��Һ��NH+4���ʵ�����ͬ | |
| B�� | 1L1mol/L��������Һ�У������Ȼ��������ΪNA | |
| C�� | ��H2O2+Cl2=2HCl+O2��Ӧ�У�ÿ����32 g��������ת��4NA������ | |
| D�� | ��ϩ�ͻ����飨C3H6����ɵ�28g��������к���3NA����ԭ�ӣ� |
| A�� | ${\;}_{81}^{203}$Tl �� ${\;}_{81}^{205}$Tl ��������ͬ | |
| B�� | ${\;}_{81}^{203}$Tl �� ${\;}_{81}^{205}$Tl��Ϊͬ�������� | |
| C�� | ${\;}_{81}^{203}$Tl �� ${\;}_{81}^{205}$Tl������֮��Ϊ2 | |
| D�� | ${\;}_{81}^{205}$Tl ԭ�Ӻ�������������������֮��Ϊ43 |
| A�� | ̼����þ��Һ���������ռ���Һ��Ӧ 2OH-+Mg2++2HCO3-=MgCO3��+CO32-+2H2Of | |
| B�� | �Ȼ����Һ�����ʯ��ˮ��Ӧ NH4++OH-=NH3��+H2O7 | |
| C�� | �⻯��������ˮ��Ӧ 2I-+Br2=I2+2Br- | |
| D�� | ��ƫ��������Һ�м���������NaHSO4��Һ AlO2-+H++H2O�TAl��OH��3�� |
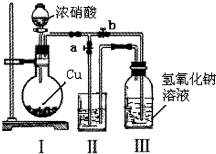 ��������������ĸ�ҹ���������������ƣ�NaNO2���������س��������ʳ�õ�˵����ij��ȤС�鿪չ����̽�����
��������������ĸ�ҹ���������������ƣ�NaNO2���������س��������ʳ�õ�˵����ij��ȤС�鿪չ����̽�����