题目内容
【题目】下列关于元素周期表中的周期、族的理解正确的是( )
A.元素周期表中每个纵列代表一个主族或副族
B.元素周期表中只有三个短周期
C.每个周期均从金属元素开始,到非金属元素结束
D.同一主族元素的最外层电子数可能不等
【答案】B
【解析】
A. Ⅷ族包括3个纵列,元素周期表中最后一个纵列为0族,0族、Ⅷ族既不是主族,也不是副族,故A错误;
B. 元素周期表中前三个周期为短周期,故B正确;
C. 第一周期仅有的两种元素均为非金属元素,故C错误;
D.同一主族元素的最外层电子数一定相等,故D错误。
故选B。

【题目】过渡元素在生活、生产和科技等方面有广泛的用途。
(1)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是________(填序号)。
A.PFS中铁显+2价
B.铁原子的价电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
Mn | Fe | ||
电离能 | I1 | 717 | 759 |
(kJ·mol-1) | I2 | 1 509 | 1 561 |
I3 | 3 248 | 2 957 |
(2)PFS中SO42-采取__________杂化,空间构型是_________。
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬与甲基丙烯酸根的配合物为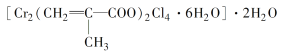
①该化合物中铬的化合价为___________。
②该化合物中一个Cr的配位数为________。
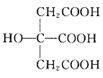
③甲基丙烯酸分子中C原子的杂化方式有___________________________________。
(4)O、S、Se为同主族元素,H2O、H2S和H2Se的参数对比见表.
化学式 | 键长/nm | 键角 |
H2O | 0.99 | 104.5° |
H2S | 1.34 | 92.3° |
H2Se | 1.47 | 91.0° |
H2S的键角大于H2Se的原因可能为__________________________________________________
【题目】化学反应速率与限度与生产、生活密切相关
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大___________。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率______________。(设溶液体积不变)
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是_________。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,3种气态物质X、Y、Z的物质的量随时间变化曲线如图。

①该反应的化学方程式是__________________________。
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是_______。
A.X、Y、Z的反应速率相等
B.容器内气体压强保持不变
C.X、Y的反应速率比为3:1
D.生成1mol Y的同时生成2mol Z
③2min内X的转化率为_____________________。