题目内容
取等物质的量浓度的NaOH溶液两份,每份为50mL。向其中各通入一定量的CO2,随后分别各取溶液10mL,将其稀释成100mL。并分别向稀释后的溶液中逐滴加入0.1mol×L-1的HCl溶液,产生的CO2气体体积(标准状况)与所加盐酸的体积之间的关系如图所示(设分别为A、B两种情况)。

回答下列问题:
(1)在(A)情况下,溶质为(写化学式)________,其物质的量之比为________,在标准状况下通入的CO2气体的体积为________。
(2)在(B)情况下,溶质为(写化学式)________,其物质的量之比为________,在标准状况下通入的CO2气体的体积为________。
(3)原NaOH溶液的物质的量浓度________。
解析:
(1)NaOH和Na2CO3,1∶1,0.27L (2)Na2CO3和NaHCO3,1∶1,0.54L (3)0.75mol/L 2NaOH+CO2=Na2CO3+H2O Na2CO3+CO2+H2O=2NaHCO3 所以在NaOH溶液中通入一定的CO2,所得溶液中的溶质可能有以下情况: ①全为Na2CO3,②全为NaHCO3,③NaOH与Na2CO3,④Na2CO3与NaHCO3。 又据:Na2CO3+HCl=NaHCO3+NaCl 1 1 1 NaHCO3+HCl=NaCl+H2O=CO2↑ 1 1 可知,若溶质为纯Na2CO3,在溶液中加入盐酸时,将Na2CO3完全转化为NaHCO3所耗HCl与将生成的NaHCO3完全转化CO2所耗HCl相等,用图象表示为:
而A中产生气体前后所用盐酸体积比为2∶1,说明溶质为NaOH与Na2CO3,而B中产生气体前后所用盐酸体积比为1∶2,说明溶质为Na2CO3与NaHCO3。
|

 阅读快车系列答案
阅读快车系列答案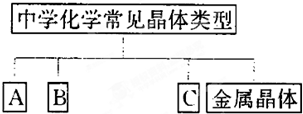
(1)完成下表,且实例按以下要求填写.
①只能由 H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3).
| A | B | C | ||
| 晶体类别 | 金属晶体 | |||
| 实例的化学式 | Na |
(3)写出上述表格中熔点最高的物质与氢氧化钠反应的化学方程式:
在理解概念的基础上,理清概念之间的相互关系,构建知识网络是学习化学的重要方法,下图是中学化学常见化学概念之间的相互关系。
 |
(1) 完成下表,且实例按以下要求填写。
①只能由H、O、N、Si、S元素中的一种或几种组成物质;②每种元素只能出现一次,化合物中最多含一种原子团;③所填物质必须能够回答问题(2)和问题(3)。
A | B | C | ||
晶体类别 | 金属晶体 | |||
实例的化学式 | Na |
(2)取上述表格中A、B、C三种晶体中某一晶体溶于水得W溶液,写出等物质的量浓度等体积的硫酸氢钠与W溶液反应的离子方程式 ;
(3)写出上述表格中熔点最高的具体物质与氢氧化钠反应的化学方程式 。
![]()

