题目内容
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,右图是它们之间的相互转化关系。请回答: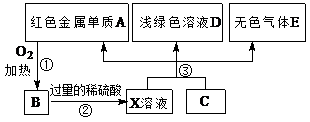
(1)反应①的基本反应类型是 ;
(2)C的化学式为 ;
(3)写出反应②的离子方程式 。
(4)A和稀硫酸、双氧水生成X的化学方程式 。
(6分)(1)化合反应(1分) (2)Fe (1分) (3) CuO+2H+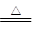 Cu2++H2O(2分)
Cu2++H2O(2分)
(4) Cu+H2O2+H2SO4="===" CuSO4+2H2O(2分)
解析试题分析:A为红色金属,可知A为铜,那么B为氧化铜;B与硫酸反应后的X溶液为硫酸和硫酸铜的混合溶液,X溶液和C反应生成了浅绿色溶液,铜和无色气体E,可知C为铁单质,我们知道浅绿色溶液应该为硫酸亚铁溶液,即D为硫酸亚铁,无色气体E为氢气。
(1 )反应①是金属铜(A)和氧气在加热条件下生成氧化铜(B),反应为2Cu+O2点燃2CuO,反应物为两种,生成物为一种,为化合反应。
(2)由于生成的溶液D为浅绿色的,所以C含有和能硫酸铜和剩余硫酸反应的物质应该是金属铁,其化学式为Fe。
(3)反应②是氧化铜和过量的硫酸反应生成硫酸铜和水,其反应方程式为:CuO+H2SO4=CuSO4+H2O,离子方程式为CuO+2H+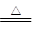 Cu2++H2O。
Cu2++H2O。
(4)由于在B中加入了过量的硫酸,导致氧化铜与硫酸反应生成硫酸铜后,硫酸依然会有剩余,所以X为硫酸铜(生成的)和硫酸(剩余的)的混合溶液.
(5)根据分析,A是铜,X是CuSO4,故A和稀硫酸、双氧水生成X的化学方程式为Cu+H2O2+H2SO4="===" CuSO4+2H2O。考点:物质的鉴别、推断
点评:此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论。

现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
形.
(3)画出C原子的电子排布图
(4)已知BA5为离子化合物,写出其电子式
(5)DE3中心原子的杂化方式为
(6)用电子式表示F元素与E元素形成化合物的形成过程
 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:

