题目内容
为证明乙醇分子中含有氧原子,可用如下装置进行实验:①各仪器所装试剂见装置图中。
②实验操作及现象:用水浴加热烧瓶A;将D中浓硫酸缓缓滴入E中与试剂Y作用,发现C中导管有大量气泡冒出;A瓶内的无水盐X逐渐变色;挥发的气体在B管口可点燃。

(1)锥形瓶E中的试剂Y应是___________。
a.饱和食盐水 b.浓盐酸 c.锌粒
(2)浓硫酸的作用:D中___________;C中___________。
(3)A瓶中发生反应的化学方程式是______________________。反应类型是___________,在B出口点燃的是生成的___________。
(4)无水盐X宜选用___________,它能起指示剂作用的原因是______________________。
(5)此实验能证明乙醇分子中含有氧原子的理由是______________________。
(1)b
(2)吸收浓盐酸中的水并放热,使HCl气体逸出 干燥HCl气体
(3)CH3CH2OH+HCl![]() CH3CH2Cl+H2O 取代反应 氯乙烷
CH3CH2Cl+H2O 取代反应 氯乙烷
(4)无水硫酸铜 无水硫酸铜是白色粉末,与水反应后会变蓝色,说明反应中有水生成
(5)无水硫酸铜变蓝色,说明反应中有水生成,水中含有氧元素,它不可能来自HCl,只能由乙醇提供
解析:由“无水盐X逐渐变色”知此无水盐为CuSO4,说明实验原理为:通过水的生成证明乙醇分子中含氧原子,即A中所发生的反应为乙醇脱—OH,通入的气体提供氢原子,—OH与—H组合成H2O,此类反应即为我们所知的:HCl+ROH![]() RCl+H2O。
RCl+H2O。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目



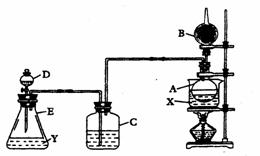 Ⅰ.装置中所装的试剂是:①A瓶装无水乙醇,内放无水盐X;②B干燥管里装生石灰;
Ⅰ.装置中所装的试剂是:①A瓶装无水乙醇,内放无水盐X;②B干燥管里装生石灰;