题目内容
下列化学方程式中电子转移不正确的是( )
A、 |
B、 |
C、 |
D、 |
考点:氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:根据化合价升降法进行判断,得出正确结论.
解答:
解:A、Cl:-1→0,↑1,×2
Mn:+4→+2,↓2,×1 共转移2个电子,故A正确;
B、Cu:0→+2,↑2,×1
N:+5→+4,↓1,×2 共转移2个电子,故B正确;
C、N:-3→0,↑3,×5
N:+5→0,↓5,×3 共转移15个电子,故C正确;
D、Cl:-1→0,↑1,×5
Cl:+5→0,↓5,×1 共转移5个电子,
应为: ,故D错误;
,故D错误;
故选:D.
Mn:+4→+2,↓2,×1 共转移2个电子,故A正确;
B、Cu:0→+2,↑2,×1
N:+5→+4,↓1,×2 共转移2个电子,故B正确;
C、N:-3→0,↑3,×5
N:+5→0,↓5,×3 共转移15个电子,故C正确;
D、Cl:-1→0,↑1,×5
Cl:+5→0,↓5,×1 共转移5个电子,
应为:
 ,故D错误;
,故D错误;故选:D.
点评:氧化还原反应是高考常见题型,每年高考中必考,是热点题型.本题考查了运用化合价升降法判断电子得失总数.

练习册系列答案
相关题目
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、31 g白磷所含共价键数目为4NA |
| B、2 L pH=1的盐酸与醋酸溶液中氢离子数均为0.2 NA |
| C、标准状况下,2.24L C4H6所含碳原子数为0.6 NA |
| D、标准状况下,22g CO2含有的电子数为0.5 NA |
NA为阿伏加德罗常数,下列叙述正确的是( )
| A、标准状态下,以任意比例混合的甲烷和丙烷的混合物22.4L,所含有的分子数约为NA |
| B、常温常压下,1mol氦气含有的质子数为4NA |
| C、体积相等的两种物质,在同温同压下,其物质的量相等 |
| D、1Lmol/L的醋酸中,所含离子数为2NA |
化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言.下列化学用语中表述正确的是( )
A、次氯酸的电子式: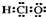 |
| B、二氧化硅的分子式:SiO2 |
C、二氧化碳的比例模型: |
D、Cl-的结构示意图: |
下列反应方程式书写正确的是( )
| A、硝酸银溶液中加入过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ |
| B、钢铁发生吸氧腐蚀的正极反应:4OH--4e-═2H2O+O2↑ |
| C、20mL 0.1mol/L AlCl3溶液中加入70mL 0.1 mol?L-1 NaOH溶液:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O |
| D、向Ba(OH)2稀溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全:Ba2++2OH-+H++SO42-+NH4+═BaSO4↓+NH3?H2O+H2O |
有相同条件下的三个反应:
①2A-+B2=2B-+A2
②2C-+A2=2A-+C2
③2B-+D2=2D-+B2
由此得出,下列判断不正确的是( )
①2A-+B2=2B-+A2
②2C-+A2=2A-+C2
③2B-+D2=2D-+B2
由此得出,下列判断不正确的是( )
| A、氧化性:D2>B2>A2>C2 |
| B、2A-+D2═2D-+A2该反应能进行 |
| C、还原性:C->A->B->D- |
| D、2B-+C2═2C-+B2该反应能进行 |
 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
 表示的分子式
表示的分子式 中含有的官能团的名称为
中含有的官能团的名称为