��Ŀ����
����Ŀ��������������ij�����Ͳ�ͬ�¶������ɵIJ�����ͼ��ʾ����֪��800���£��ݻ��̶����ܱ������з�����Ӧ�١��ڣ�
4NH3��g��+3O2��g�� ![]() 2N2��g��+6H2O��g������
2N2��g��+6H2O��g������
4NH3��g��+5O2��g�� ![]() 4NO��g��+6H2O��g������
4NO��g��+6H2O��g������
����������˵������Ӧ���ﵽƽ����ǣ� ��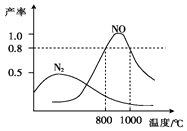
A.v��N2��=v��NO��
B.��Ӧ�ٵ��ʱ��H���ֺ㶨
C.��ϵ���ܶȲ��ٷ����仯
D.��������ƽ����Է����������ٷ����仯
���𰸡�D
���������⣺A��v��N2��=v��NO����δ�������淴Ӧ�Ĺ�ϵ����A����
B��ֻҪ��ѧ����ʽ���䣬���H���ֺ㶨����ƽ��״̬�أ���B����
C������������䣬��Ӧǰ�������壬��������ʼ�ղ��䣬˵���ܶ�ʼ�ղ��䣬�ܶȲ��䲻��˵����Ӧ�ﵽƽ��״̬����C����
D����������ƽ����Է����������ٷ����仯��˵���������ʵ������䣬�Ѵ�ƽ�⣬��D��ȷ��
��ѡD��
�����㾫����������Ĺؼ��������⻯ѧƽ��״̬���ʼ����������֪ʶ�����ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����

 �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
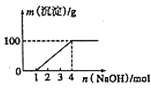
Сѧ�̲���ȫ���ϵ�д�����Ŀ��ij��ɫϡ��ҺX�У����ܺ���������������е�ij���֣�ȡ����Һ�����������м���ij�Լ�Y���������������ʵ�����n��������Լ������y���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
������ | CO32����SiO32����[Al��OH��4]����Cl�� |
������ | Al3+��Fe3+��Mg2+��NH4+��Na+ |
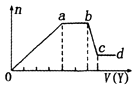
A.��Y�����ᣬ��X��һ������CO32����SiO32����[Al��OH��4]����NH4+
B.��Y��NaOH��Һ����X��һ������A13+��Fe3+��NH4+��Cl��
C.��Y��NaOH��Һ����ab�η�����Ӧ�����ӷ���ʽΪ��NH4++OH���TNH3��+H2O
D.��Y��NaOH��Һ����X�е�Al3+��Mg2+��NH4+���ʵ���֮��Ϊ2��1��4