题目内容
下列叙述正确的是( )
| A、将5.85gNaCl晶体溶入100mL水中,制得0.1mol/L的NaCl溶液 |
| B、通常状况下,1 NA 个SO2分子占有的体积为22.4L |
| C、用四氯化碳萃取碘水中的碘,充分振荡后静置下层溶液为紫色 |
| D、将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L |
考点:物质的量的相关计算
专题:计算题
分析:A.溶剂的体积不等于溶液的体积;
B.标准状况下,1mol气体的体积约为22.4L;
C.四氯化碳的密度比水大;
D.根据溶液稀释前后溶质的物质的量不变.
B.标准状况下,1mol气体的体积约为22.4L;
C.四氯化碳的密度比水大;
D.根据溶液稀释前后溶质的物质的量不变.
解答:
解:A.5.85gNaCl的物质的量为0.1mol,但溶剂的体积不等于溶液的体积,故A错误;
B.标准状况下,1mol气体的体积约为22.4L,通常状况下,1 NA 个SO2分子占有的体积大于22.4L,故B错误;
C.碘易溶于四氯化碳,四氯化碳的密度比水大,则用四氯化碳萃取碘水中的碘,充分振荡后静置下层溶液为紫色,故C正确;
D.溶液稀释前后溶质的物质的量不变,则将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L,故D正确.
故选CD.
B.标准状况下,1mol气体的体积约为22.4L,通常状况下,1 NA 个SO2分子占有的体积大于22.4L,故B错误;
C.碘易溶于四氯化碳,四氯化碳的密度比水大,则用四氯化碳萃取碘水中的碘,充分振荡后静置下层溶液为紫色,故C正确;
D.溶液稀释前后溶质的物质的量不变,则将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L,故D正确.
故选CD.
点评:本题考查较为综合,涉及物质的量的计算、萃取等知识,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意相关计算公式的运用以及相关概念的理解,难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
下列离子方程式书写正确的是( )
| A、澄清的石灰水与醋酸反应:OH-+CH3COOH=CH3COO-+H2O |
| B、碳酸钙与盐酸反应:CO2-3+2H+═CO2↑+H2O |
| C、钠与水反应:Na++H2O═Na++OH-+H2↑ |
| D、铜片与硝酸银溶液反应:Cu+Ag+═Cu2++Ag |
下列物质属于酚类的是( )
A、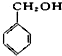 |
B、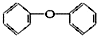 |
C、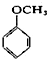 |
D、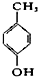 |
下列离子方程式书写正确的是( )
| A、AlCl3溶液与过量的氨水反应:Al3++3OH-=Al(OH)3↓ |
| B、工业上用NO2与水反应制取HNO3:3NO2+H2O═NO3-+NO+2H+ |
| C、碳酸氢钠溶液与稀硫酸反应:HCO3-+H+=CO2↑+H2O |
| D、硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓ |
下列说法不正确的是( )
| A、油脂会造成人体肥胖,所以不能食用 |
| B、脂肪酸在体内可以被氧化从而供给人体热量 |
| C、摄入人体的脂肪大部分成为脂肪组织存在于人体内 |
| D、必需脂肪酸在体内有促进发育、维持健康和参与胆固醇代谢的生理功能 |
铅笔芯的主要成分是石墨.如果铅笔芯写一个字消耗的石墨质量约为1×10-3g,那么一个铅笔字含有的碳原子数约为( )
| A、5×1019个 |
| B、5×1022个 |
| C、2.5×1022个 |
| D、2.5×1019个 |
防治环境污染,改善生态环境已成为全球的共识.下列措施有利于改善环境质量的是( )
| A、利用太阳能、潮汐能、风力发电,以获取清洁能源 |
| B、将废电池深埋,以减少重金属的污染 |
| C、将地沟油回收再加工为食用油,以减缓水体富营养化 |
| D、利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯 |
能正确解释下列反应原理的离子方程式是( )
| A、用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+ |
| B、用小苏打治疗胃酸过多:CO32-+2H+=CO2↑+H2O |
| C、用氯化铁溶液腐蚀印刷线路板上的铜:Fe3++Cu=Fe2++Cu2+ |
| D、FeCl3溶液中撒入CaCO3粉末有气泡产生:2Fe3++3CaCO3+3H2O=2Fe(OH)3↓+3Ca2++3CO2↑ |