题目内容
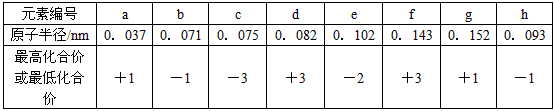
现有八种短周期元素a—h的有关性质的数据如下:元素编号 | a | b | c | d | e | f | g | h |
原子半?径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或最低化合价 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
根据元素周期律,判断下列推断不正确的是
A.元素a与元素c形成的化合物分子中的化学键是极性键
B.b元素形成的氢化物分子间存在氢键
C.e元素位于周期表中的第二周期ⅥA族
D.元素f的最高价氧化物的水化物能溶于元素h的最高价氧化物的水溶液中
C
解析:对短周期元素而言,其最高正化合价为该元素原子的最外层电子数即族序数,其最低负化合价与8之和即为该元素原子的最外层电子数;同周期从左到右原子半径逐渐减小,同主族由上到下原子半径逐渐增大。结合表中数据,易推知a为H,b为F,c为N,e为S,f为Al,h为Na。NH3分子只存在极性键,HF分子间易形成氢键,Al(OH)3为典型的两性氢氧化物,能与NaOH溶液反应。

练习册系列答案
相关题目
现有八种短周期元素a—h的有关性质的数据如下:
元素编号 | a | b | c | d | e | f | g | h |
原子半径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
最高化合价或最低化合价 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
根据元素周期律,判断下列推断不正确的是( )
A.元素a与元素c形成的化合物分子中的化学键是极性键
B.b元素形成的氢化物分子间存在氢键
C.e元素位于元素周期表中的第二周期VIA族
D.元素f的最高价氧化物的水化物能溶于元素h的最高价氧化物的水化物的水溶液中

 2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.
2SO3(g);△H=-196.6KJ?mol-1.平衡时容器内气体压强为起使时的90%.