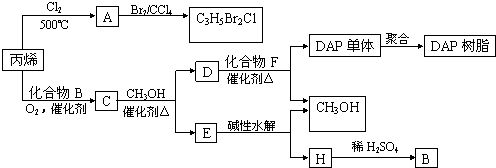
题目内容
(1)HCl的相对分子质量为
(2)0.5mol的Fe含
(3)在标准状况下:0.5mol HCl气体占有的体积约为
(4)100mL 1mol?L-1 氯化铝溶液中Al3+的物质的量为
36.5
36.5
,HCl的摩尔质量为36.5g?mol-1
36.5g?mol-1
,49g H2SO4的物质的量为0.5mol
0.5mol
;(2)0.5mol的Fe含
0.5NA
0.5NA
个铁原子,质量是28
28
g,12.04×1023个铁原子约是2
2
mol.(3)在标准状况下:0.5mol HCl气体占有的体积约为
11.2L
11.2L
,33.6L H2的物质的量是1.5mol
1.5mol
,16g O2的体积是11.2L
11.2L
.44.8L N2中含有的N2分子数是2NA
2NA
.(4)100mL 1mol?L-1 氯化铝溶液中Al3+的物质的量为
0.1mol
0.1mol
,Al3+的浓度为1mol?L-1
1mol?L-1
,Cl-的浓度为3mol?L-1
3mol?L-1
,与300mL 1mol?L-1 氯化钠溶液中Cl-的浓度相同否
否
(填“是”或“否”).分析:根据n=
=
=
=cV结合物质的构成计算相关物理量.
| m |
| M |
| N |
| NA |
| V |
| Vm |
解答:解:(1)HCl的相对分子质量为36.5;摩尔质量为36.5g?mol-1;49g H2SO4的物质的量为
=0.5mol,
故答案为:36.5;36.5g?mol-1;0.5mol;
(2)N(Fe)=0.5mol×NA/mol=0.5NA;m(Fe)=0.5mol×56g/mol=28g;n(Fe)=
=2mol,
故答案为:0.5NA;28;2;
(3)0.5mol HCl气体占有的体积约为0.5mol×22.4L/mol=11.2L;33.6LH2的物质的量是
=1.5mol;
16gO2的体积是
×22.4L/mol=11.2L;44.8LN2中含有的N2分子数是
×NA/mol=2NA,
故答案为:11.2L;1.5mol;11.2L;2NA;
(4)氯化铝溶液中Al3+的物质的量为0.1L×1mol?L-1=0.1mol;Al3+的浓度为1mol?L-1;Cl-的浓度为3mol?L-1;1mol?L-1 氯化钠溶液中Cl-的浓度为1mol?L-1,两种溶液中Cl-浓度不同,
故答案为:0.1mol;1mol?L-1;3mol?L-1;否.
| 49g |
| 98g/mol |
故答案为:36.5;36.5g?mol-1;0.5mol;
(2)N(Fe)=0.5mol×NA/mol=0.5NA;m(Fe)=0.5mol×56g/mol=28g;n(Fe)=
| 12.04×1023 |
| 6.02×1023/mol |
故答案为:0.5NA;28;2;
(3)0.5mol HCl气体占有的体积约为0.5mol×22.4L/mol=11.2L;33.6LH2的物质的量是
| 33.6L |
| 22.4L/mol |
16gO2的体积是
| 16g |
| 32g/mol |
| 44.8L |
| 22.4L/mol |
故答案为:11.2L;1.5mol;11.2L;2NA;
(4)氯化铝溶液中Al3+的物质的量为0.1L×1mol?L-1=0.1mol;Al3+的浓度为1mol?L-1;Cl-的浓度为3mol?L-1;1mol?L-1 氯化钠溶液中Cl-的浓度为1mol?L-1,两种溶液中Cl-浓度不同,
故答案为:0.1mol;1mol?L-1;3mol?L-1;否.
点评:本题考查物质的量的相关计算,题目难度不大,注意把握相关计算公式的运用,答题时注意思路的形成.

练习册系列答案
相关题目

 )
)
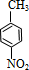
 +HOCH2CH2Cl
+HOCH2CH2Cl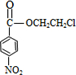 +H2O
+H2O




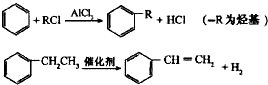
 +CH3CH2Cl
+CH3CH2Cl +HCl
+HCl