题目内容
实验探究:固体反应物表面积跟反应速率的关系.
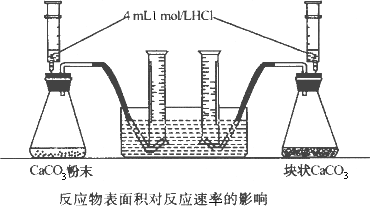
本实验控制的变量有哪些?通过什么现象说明反应速率的快慢?
答案:
解析:
解析:
|
答案:控制盐酸的量相等而且不足,控制碳酸钙的质量相等且同温.产生气体的快慢可以从排水的速率看出来. 思路与技巧:本实验控制盐酸的量相等而且不足,这样可以产生等量的二氧化碳,控制碳酸钙的质量相等,但其中一个碳酸钙用粉末,这样与液体的接触面积大,从而观察产生气体的快慢,产生气体的快慢可以从排水的速率看出来. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
