题目内容
14.相同质量的下列气体中电子数最少的是( )| A. | O2 | B. | Cl2 | C. | N2 | D. | CO2 |
分析 根据n=$\frac{m}{M}$,结合分子所含电子数分析解答.
解答 解:设气体的质量都为1g,
A、氧气的物质的量为:$\frac{1g}{32g/mol}$,所以含电子数为:$\frac{1g}{32g/mol}$×16=0.5mol;
B、氯气的物质的量为:$\frac{1g}{71g/mol}$,所以含电子数为:$\frac{1g}{71g/mol}$×34=0.49mol;
C、氮气的物质的量为:$\frac{1g}{28g/mol}$,所以含电子数为:$\frac{1g}{28g/mol}$×14=0.5mol;
D、二氧化碳的物质的量为:$\frac{1g}{44g/mol}$,所以含电子数为:$\frac{1g}{44g/mol}$×22=0.5mol;综上电子数最少的是B,故选B.
点评 本题考查物质的量的有关计算,题目难度不大,注意根据物质的量和气体的分子组成计算电子数目的多少.

练习册系列答案
相关题目
9.阅读、分析下列两个材料:
材料一、如图
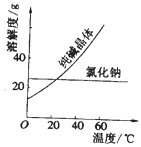
材料二
回答下列问题:
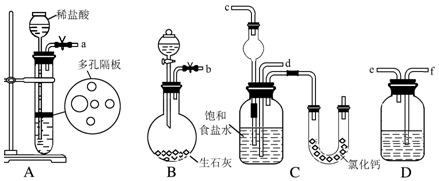
(1)要从氯化钠和纯碱的固体混合物中分离得到纯净的氯化钠,应先将固体溶解,再经过蒸发结晶趁热过滤、洗涤、干燥等操作.
(2)将乙二醇和丙三醇相互分离的最佳方法是蒸馏法,写出该方法在操作上的注意事项(写出一项)蒸馏烧瓶中应加入沸石.
材料一、如图

材料二
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
(1)要从氯化钠和纯碱的固体混合物中分离得到纯净的氯化钠,应先将固体溶解,再经过蒸发结晶趁热过滤、洗涤、干燥等操作.
(2)将乙二醇和丙三醇相互分离的最佳方法是蒸馏法,写出该方法在操作上的注意事项(写出一项)蒸馏烧瓶中应加入沸石.
8.某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如(见表格),请结合表中信息,回答有关问题:
(1)写出上述反应的离子方程式S2O32-+2H+═S↓+SO2↑+H2O.
(2)在利用比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件.其中:
①能说明温度对该反应速率影响的组合比较是BD;(填实验序号)
②A和B、A和C的组合比较所研究的问题是相同温度条件下浓度对该反应速率的影响;
(3)教材是利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:SO2可溶于水,测定不精确或实验装置较复杂,不易控制.
| 实验 序号 | 反应温度 (℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
(2)在利用比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件.其中:
①能说明温度对该反应速率影响的组合比较是BD;(填实验序号)
②A和B、A和C的组合比较所研究的问题是相同温度条件下浓度对该反应速率的影响;
(3)教材是利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:SO2可溶于水,测定不精确或实验装置较复杂,不易控制.


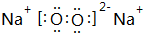 ;
;