题目内容
在FeCl3,CuCl2,FeCl2的混合溶液中,Fe3+,Cu2+和Fe2+的物质的量之比为3∶2∶1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变化为1∶2∶4,则参加反应的铁粉与原溶液Fe3+的物质的量之比为
A.2∶1 B.1∶2 C.1∶3 D.1∶4
C
【解析】
试题分析:因氧化性:Fe3+>Cu2+>Fe2+,加入适量的铁粉,使溶液中Fe3+、Cu2+和Fe2+物质的量之比变为1:2:4,说明Fe3+有剩余,则Cu2+没有参加反应,加入Fe粉仅与反应Fe3+,
设原溶液中含有Fe3+、Cu2+、Fe2+的物质的量分别为3mol、2mol、1mol,反应后Fe3+、Cu2+和Fe2+物质的量之比变为1:2:4,则反应后Fe3+、Cu2+、Fe2+的物质的量分别为1mol、2mol、4mol,故反应的Fe3+的物质的量为3mol-1mol=2mol,则:
2Fe3++Fe=3Fe2+
2mol 1mol 3mol
故参加反应的Fe的物质的量为1mol,
参加反应的铁粉与原溶液中Fe2+的物质的量之比为1mol:3mol=1:3;
考点:有关混合物的计算

 阅读快车系列答案
阅读快车系列答案已知25。C时,下表为几种常见物质的溶度积常数;下列有关说法不正确的是( )
化学式 | 溶度积常数 | 化学式 | 溶度积常数 |
Ag2S | 6.3×10-50 | AgCl | 1.8×10-10 |
CuS | 4.3×10-36 | AgBr | 5.4×10-13 |
FeS | 6.3×10-18 | AgI | 8.3×10-17 |
A.除去工业废水中的Cu2+可以选用Na2S作沉淀剂
B.将AgCl、AgBr和AgI饱和溶液等体积混合后,再加入足量的浓AgNO3溶液,首先析出AgI沉淀
C.Ag2S、CuS、FeS溶解度依次增大
D.将FeS加入较浓的CuSO4溶液中,会有CuS生成

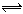 2C+2D,在4种不同情况下的反应速率分别为单位mol·Lˉ1·sˉ1:
2C+2D,在4种不同情况下的反应速率分别为单位mol·Lˉ1·sˉ1: