题目内容
常温下,浓度均为0.1mol?L-1的三种溶液:①醋酸溶液②醋酸钠溶液③碳酸钠溶液.下列说法正确的是( )
分析:A、强电解质的电离程度大于等浓度的弱电解质的电离程度;
B、醋酸显示酸性,醋酸钠和碳酸钠水解显示碱性,水解程度大,碱性强;
C、酸对水的电离起到抑制作用,盐的水解对水的电离起到促进作用,水解程度大,对水的电离促进作用越大;
D、水的离子积只受温度的影响,温度不变,水的离子积不变.
B、醋酸显示酸性,醋酸钠和碳酸钠水解显示碱性,水解程度大,碱性强;
C、酸对水的电离起到抑制作用,盐的水解对水的电离起到促进作用,水解程度大,对水的电离促进作用越大;
D、水的离子积只受温度的影响,温度不变,水的离子积不变.
解答:解:A、强电解质的电离程度大于等浓度的弱电解质的电离程度,所以浓度均为0.1mol?L-1的醋酸溶液和醋酸钠溶液,c(CH3COO-):①<②,故A错误;
B、醋酸显示酸性,醋酸钠和碳酸钠水解显示碱性,但是碳酸钠的水解程度大,所以碳酸钠pH大碱性强,溶液的pH:①<②<③,故B错误;
C、醋酸对水的电离起到抑制作用,能水解的盐对水的电离起到促进作用,碳酸钠水解程度大,对水的电离促进作用越大,所以水的电离程度:①<②<③,故错正确;
D、水的离子积只受温度的影响,温度不变,水的离子积不变,所以水的离子积:①=②=③,故D错误.
故选:C.
B、醋酸显示酸性,醋酸钠和碳酸钠水解显示碱性,但是碳酸钠的水解程度大,所以碳酸钠pH大碱性强,溶液的pH:①<②<③,故B错误;
C、醋酸对水的电离起到抑制作用,能水解的盐对水的电离起到促进作用,碳酸钠水解程度大,对水的电离促进作用越大,所以水的电离程度:①<②<③,故错正确;
D、水的离子积只受温度的影响,温度不变,水的离子积不变,所以水的离子积:①=②=③,故D错误.
故选:C.
点评:本题考查学生弱电解质的电离以及盐的水解知识,注意弱离子水解程度规律:越弱越水解的应用.

练习册系列答案
相关题目
 运用化学知识解决生产、生活中的有关问题备受关注.请回答下列问题:
运用化学知识解决生产、生活中的有关问题备受关注.请回答下列问题: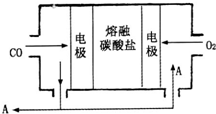 (2013?德州模拟)钠及其化合物具有广泛的用途.
(2013?德州模拟)钠及其化合物具有广泛的用途.