题目内容
13.A、B、C、D、E是五种短周期元素,A的某种原子失去一个电子后可形成一个质子,B的某种单质是自然界中最硬的物质,C的某种单质是生物呼吸必需的气体,D元素原子的K层和M层电子数相同,E是短周期金属性最强的元素.下列说法正确的是( )| A. | C、D、E的简单离子半径由大到小的顺序是E>D>C | |
| B. | 含有E的盐溶液可能显酸性、可能显中性、也可能显碱性 | |
| C. | A和C形成的化合物中一定只有极性键 | |
| D. | BC2跟C、E形成的化合物发生的反应都是非氧化还原反应 |
分析 A的某种原子失去一个电子后可形成一个质子,应为H元素,B的某种单质是自然界中最硬的物质,为C元素,C的某种单质是生物呼吸必需的气体,为O元素,D元素原子的K层和M层电子数相同,为Mg元素,E是短周期金属性最强的元素,为Na元素,结合对应的单质、化合物的性质以及元素周期律解答该题.
解答 解:由以上分析可知A为H、B为C、C为O、D为Mg、E为Na元素.
A.C、D、E的简单离子具有相同的核外电子排布,核电荷数越大离子半径越小,故A错误;
B.E为Na元素,对应的盐溶液如为NaCl等,则为中性,如为NaClO等,则呈碱性,如为NaHSO4等,则呈酸性,故B正确;
C.A和C形成的化合物如为H2O2,则既含极性键又含非极性键,故C错误;
D.如为CO2与Na2O2的反应,则为氧化还原反应,故D错误.
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的性质推断元素为解答本题的关键,侧重分析与应用的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
相关题目
3.工业废气H2S经资源利用后可回收能量并得到单质硫.反应原理如图所示.下列说法不正确的是( )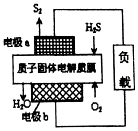

| A. | 电极a为电池的负极 | |
| B. | 电极b上发生的电极反应为O2+4H++4e-═2H2O | |
| C. | 若电路中通过2mol电子,则电池内部释放632kJ热量 | |
| D. | 若有17gH2S参与反应,则会有1molH+经质子膜进入正极区 |
4.工业上用含锰废料(主要成分MnO2,含有少量Fe2O3、Al2O3、CuO、CaO等)与烟气脱硫进行联合处理并制备MnSO4的流程如图1:

已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如表所示.
请回答:
(1)沉淀1的化学式为CaSO4.
(2)(NH4)2S的电子式为 ;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.
;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.
(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为.
(4)已知:滤液3中除MnSO4外,还含有少量(NH4)2SO4.(NH4)2SO4、MnSO4的溶解度曲线如图2所示.
据此判断,操作“I”应为蒸发浓缩、趁热过滤、洗涤、干燥.
(5)工业上可用电解酸性MnSO4溶液的方法制备MnO2,其阳极反应式为Mn2++2H2O-2e-=MnO2+4H+.
(6)25.35g MnSO4•H2O样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如图3所示.
①300℃时,所得固体的化学式为MnSO4.
②1150℃时,反应的化学方程式为3MnO2$\frac{\underline{\;1150℃\;}}{\;}$Mn3O4+O2↑.

已知:25℃时,部分氢氧化物的溶度积常数(Ksp)如表所示.
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| Ksp | 1.0×10-33 | 4.0×10-38 | 2.0×10-20 | 4.0×10-14 |
(1)沉淀1的化学式为CaSO4.
(2)(NH4)2S的电子式为
 ;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.
;“净化”时,加入(NH4)2S的作用为使Cu2+转化为CuS沉淀.(3)“酸化、还原”中,发生的所有氧化还原反应的离子方程式为.
(4)已知:滤液3中除MnSO4外,还含有少量(NH4)2SO4.(NH4)2SO4、MnSO4的溶解度曲线如图2所示.
据此判断,操作“I”应为蒸发浓缩、趁热过滤、洗涤、干燥.
(5)工业上可用电解酸性MnSO4溶液的方法制备MnO2,其阳极反应式为Mn2++2H2O-2e-=MnO2+4H+.
(6)25.35g MnSO4•H2O样品受热分解过程的热重曲线(样品质量随温度变化的曲线)如图3所示.
①300℃时,所得固体的化学式为MnSO4.
②1150℃时,反应的化学方程式为3MnO2$\frac{\underline{\;1150℃\;}}{\;}$Mn3O4+O2↑.
1.用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示.下列说法不正确的是( )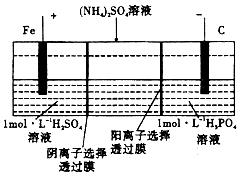

| A. | 阳极室溶液由无色变成浅绿色 | |
| B. | 当电路中通过lmol电子的电量时,阴极有0.5mol的气体生成 | |
| C. | 电解时中间室(NH4)2SO4溶液浓度下降 | |
| D. | 电解一段时间后,阴极室溶液中的溶质一定是(NH4)3PO4 |
8.化学与生产、生活、社会发展等息息相关,下列说法正确的是( )
| A. | “可燃冰”被认为是21世纪新型洁净的能源,但大量开发和使用会诱发海底地质灾害,还会加重温室效应 | |
| B. | 碘元素被誉为“智力元素”,KI、KIO3、I2都可作碘盐的添加剂 | |
| C. | 硅橡胶无毒无味、耐高温又耐低温,可制成人造心脏,它属于无机非金属材料 | |
| D. | “雾霾天气”“温室效应”“光化学烟雾”的形成都与氮的氧化物无关 |
18.化学与社会、生活密切相关.对下列现象或事实的解释中正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 液氨可用作制冷剂 | NH3的化学性质稳定,不易发生反应 |
| B | 小苏打片用于治疗胃酸过多 | Na2CO3能与盐酸反应,降低胃液的酸度 |
| C | SO2可用作葡萄酒的食品添加剂 | SO2具有漂白性,能杀菌、消毒 |
| D | Al(OH)3用作塑料等材料的阻燃剂 | 受热易分解生成Al2O3和H2O,同时吸收热量 |
| A. | A | B. | B | C. | C | D. | D |
5.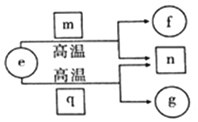 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径的大小:W>Z>X | |
| B. | 简单氢化物的沸点:W>Y>Z | |
| C. | 元素Y、Z、W形成的单质不止一种 | |
| D. | 元素Y、Z、W与元素X均能形成18e-的分子 |
2.两种气态烃的混合物共2.24L(标准状况下),完全燃烧后得3.36L(标准状况下)二氧化碳和3.6g的水.下列说法中,正确的是( )
| A. | 混合气体中一定含有甲烷 | B. | 混合气体中一定含有乙烯 | ||
| C. | 混合气体中一定含有甲烷和乙烯 | D. | 混合气体中一定含有乙烷 |
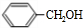 ;
;