题目内容
15. 如图进行实验,向试管中的b溶液中加入少量a溶液,试管中现象对应的离子方程式正确的是( ))
如图进行实验,向试管中的b溶液中加入少量a溶液,试管中现象对应的离子方程式正确的是( ))| 选项 | a | b | 试管中现象 | 离子方程式 |
| A | 稀H2SO4 | KI淀粉 | 在空气中放置一段时间后溶液呈黄色 | 4I-+O2+2H2O=2I2+4OH- |
| B | Na2CO3 | 稀盐酸 | 开始时无气泡,后来有气泡 | CO32-+H+=HCO3-; HCO3-+H+=H2O+CO2↑ |
| C | 稀盐酸 | Na2SiO3 | 产生白色胶状物 | 2H++SiO32-=H2SiO3(胶体) |
| D | 稀H2SO4 | 滴有酚酞的Ba(OH)2 | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-= BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.碘单质遇到淀粉显示蓝色,不是黄色,且反应产物中不会有氢氧根离子;
B.将碳酸钠加入稀盐酸中,开始就会生成气体;
C.硅酸钠与盐酸反应生成白色的硅酸胶体;
D.离子方程式错误,氢离子与氢氧根离子的系数与硫酸、氢氧化钡的化学式组成不相符.
解答 解:A.酸性条件下碘离子容易被氧气氧化成碘单质,发生反应为:4I-+O2+4H+=2H2O+2I2,碘单质遇到淀粉显示蓝色,不是黄色,反应产物中不会有氢氧根离子,故A错误;
B.将碳酸钠溶液加入盐酸中,酸过量,开始就产生气泡,反应的离子方程式为:CO32-+2H+=H2O+CO2↑,故B错误;
C.Na2SiO3与盐酸反应的离子方程式为:2H++SiO32-=H2SiO3(胶体),所以会生成白色胶状物,故C正确;
D.氢氧化钡与稀硫酸反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,题中离子方程式错误,故D错误;
故选C.
点评 本题考查了离子方程式的书写判断,为高考的高频题,题目难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
5.N2O俗称“笑气”,曾用作可吸入性麻醉剂,下列反应能产生N2O:3CO+2NO2═3CO2+N2O.下列关于N2O的说法一定正确的是( )
| A. | 等物质的量的N2O和CO2含有相等的电子数 | |
| B. | N2O只有氧化性,无还原性 | |
| C. | 上述反应,每生成l mol N2O,消耗1.5 mol CO | |
| D. | N2O会迅速与人体血红蛋白结合,使人中毒 |
6.下列说法不正确的是( )
| A. | 探究温度对反应速率影响时,分别水浴加热硫代硫酸钠溶液、硫酸溶液到一定温度,再将两溶液混合 | |
| B. | 用简易量热计测定反应热,使用碎泡沫隔热保温、环形玻璃搅拌棒搅拌、量取达到的最高温度,计算反应热,取2~3 次的实验平均值 | |
| C. | H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 | |
| D. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)分别为中和滴定实验和pH试纸 |
3.下列溶液中,能用来区别SO2和CO2气体的是( )
①石灰水 ②H2S溶液 ③KMnO4溶液 ④紫色石蕊溶液 ⑤BaCl2溶液 ⑥品红溶液.
①石灰水 ②H2S溶液 ③KMnO4溶液 ④紫色石蕊溶液 ⑤BaCl2溶液 ⑥品红溶液.
| A. | ①④⑤ | B. | ②④⑤ | C. | ③④⑤ | D. | ②③⑥ |
10.下列有关试剂的保存方法,不正确的是( )
| A. | 浓硝酸保存在棕色试剂瓶中 | B. | 少量金属钠可保存在煤油里 | ||
| C. | 新制氯水保存在棕色试剂瓶中 | D. | 浓硫酸保存在橡胶塞试剂瓶中 |
20.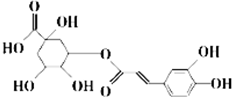 中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
 中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )
中成药银翘中含有具有较广泛抗菌作用的有效成分--绿原酸,其结构简式如图所示.下列有关说法不正确的是( )| A. | 绿原酸可通过酯化反应人工合成 | |
| B. | 1 mol绿原酸能与2molBr2发生加成反应 | |
| C. | 1mol绿原酸能与6molNa发生置换反应 | |
| D. | 绿原酸能与NaHCO3溶液发生复分解反应 |
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工厂通常采用20 Mpa~50 MPa压强,以提高原料的利用率 | |
| C. | 打开啤酒瓶盖后有大量泡沫溢出 | |
| D. | 夏天将食品储藏在冰箱中 |
4.在2A(g)+B(g)?3C(g)+4D(g)反应中,表示该反应速率最快的是( )
| A. | υ(A)=0.5 mol/(L•min) | B. | υ(B)=0.3 mol/(L•min) | ||
| C. | υ(C)=0.03 mol/(L•s) | D. | υ(D)=1 mol/(L•min) |
8.下列酸性条件下离子能大量共存的是( )
| A. | Na+、K+、CO32-、SO42- | B. | Cu2+、SO42-、HCO3-、Na+ | ||
| C. | Cu2+、SO42-、NO3-、Fe3+ | D. | OH-、Na+、Mg2+、SO42- |