题目内容
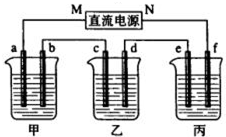
甲、乙、丙三个烧杯中分别装有稀硫酸、氯化铜溶液、饱和食盐水,把用导线连接的锌片和铜片插入甲,把分别与直流电流正、负极相连的C1、C2插入乙,把分别与直流电源正、负极相连的C3、铁片插入丙.则下列叙述正确的是( )
| A、甲、丙中是化学能转变为电能,乙中是电能转变为化学能 | B、C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 | C、C1和C3放出的气体相同,铜片和铁片放出的气体也相同 | D、甲、乙中溶液的pH值逐渐升高,丙中溶液的pH逐渐减小 |
分析:甲构成原电池,锌易失电子作负极,铜作正极;乙是电解池,C1作阳极,C2作阴极,阳极上氯离子放电生成氯气,阴极上铜离子放电生成铜;丙是电解池,C3作阳极,铁片作阴极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,据此分析解答.
解答:解:A.甲没有外接电源,是将化学能转化为电能的装置,属于原电池;乙和丙有外接电源,是将电能转化为化学能的装置,属于电解池,故A错误;
B.乙是电解池,C1作阳极,C2作阴极,锌失电子发生氧化反应,铁片上得电子发生还原反应,故B错误;
C.C1和C3放出的气体都是氯气,铜片和铁片上都是氢离子放电生成氢气,故C正确;
D.甲溶液由酸逐渐变为盐,pH逐渐增大;乙中析出氯气和铜,溶液由弱酸性逐渐变为中性,则pH增大,丙溶液析出氯气和氢气,同时溶液中生成氢氧化钠,溶液的pH逐渐增大,故D错误;
故选:C.
B.乙是电解池,C1作阳极,C2作阴极,锌失电子发生氧化反应,铁片上得电子发生还原反应,故B错误;
C.C1和C3放出的气体都是氯气,铜片和铁片上都是氢离子放电生成氢气,故C正确;
D.甲溶液由酸逐渐变为盐,pH逐渐增大;乙中析出氯气和铜,溶液由弱酸性逐渐变为中性,则pH增大,丙溶液析出氯气和氢气,同时溶液中生成氢氧化钠,溶液的pH逐渐增大,故D错误;
故选:C.
点评:本题考查了原电池和电解池原理,明确正负极及阴阳极上生成的物质是解本题关键,难点是确定溶液pH的变化,根据溶液中溶质的变化来分析解答即可,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放109g5.51%的NaOH溶液、足量的CuSO4溶液和200g10.00%的K2SO4溶液.电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放109g5.51%的NaOH溶液、足量的CuSO4溶液和200g10.00%的K2SO4溶液.电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加.据此回答问题: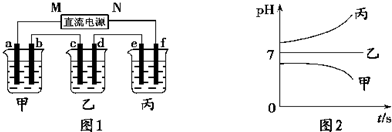


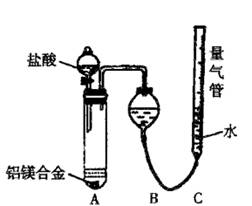
 (一)甲组:实验方案:镁铝合金
(一)甲组:实验方案:镁铝合金 测定剩余固体质量
测定剩余固体质量 盘天平称量一定质量镁铝合金粉末
盘天平称量一定质量镁铝合金粉末 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 测定生成气体的体积
测定生成气体的体积

 并最终得到固体物质1.45g。则该合金中铝的质量分数为 。
并最终得到固体物质1.45g。则该合金中铝的质量分数为 。 测定剩余固体质量
测定剩余固体质量 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 测定生成气体的体积
测定生成气体的体积