题目内容
下列变化中,需加氧化剂才能实现的是
- A.CO2→CO32-
- B.C→CO2
- C.FeCl3→FeCl2
- D.HCl→MgCl2
分析:需加氧化剂才能实现,则选项中为还原剂的氧化反应,还原剂中某元素的化合价升高,以此来解答.
解答:A.CO2→CO32-中,C元素的化合价不变,不发生氧化还原反应,故A不选;
B.C→CO2中,C元素的化合价升高,需价氧化剂,故B选;
C.FeCl3→FeCl2中,Fe元素的化合价降低,需加还原剂,故C不选;
D.HCl→MgCl2中,Cl元素的化合价不变,发生复分解反应可以实现,故D不选;
故选B.
点评:本题考查氧化还原反应,明确反应中元素的化合价及基本概念即可解答,注意还原剂中某元素的化合价升高,题目难度不大.

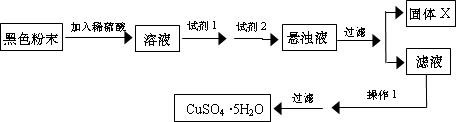
(15分)硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。
Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:

|
棉球 |
棉球上滴加的试剂 |
实验现象 |
解释和结论 |
|
a |
|
棉球变白,微热后又恢复红色 |
|
|
b |
含酚酞的NaOH溶液 |
棉球变为白色 |
离子方程式: |
|
c |
|
棉球变为白色 |
该气体具有 (选填“氧化性”或“还原性”) |
Ⅱ、硬质玻璃管与其它装置结合完成定性或定量实验。下图是某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究的装置。

实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定

(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
a.滴定管用蒸馏水洗涤后再用待装液润洗
b.锥形瓶需要用待测液润洗
c.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为
 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.


 )是一种医药中间体.某兴趣小组提出用茴香醛(
)是一种医药中间体.某兴趣小组提出用茴香醛(  )为基本原料通过2步合成E.指出该流程中所涉及的化学反应类型
)为基本原料通过2步合成E.指出该流程中所涉及的化学反应类型


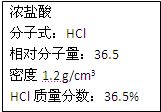 右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: