题目内容
铁与盐溶液反应:
(1)铁和氯化铜溶液:化学方程式: ;离子方程式: ;
(2)除去FeCl2溶液中的FeCl3:化学方程式: ;离子方程式: .
(1)铁和氯化铜溶液:化学方程式:
(2)除去FeCl2溶液中的FeCl3:化学方程式:
考点:铁的化学性质
专题:几种重要的金属及其化合物
分析:(1)铁和氯化铜溶液反应生成氯化亚铁和铜;
(2)除去FeCl2溶液中的FeCl3,可加入铁粉.
(2)除去FeCl2溶液中的FeCl3,可加入铁粉.
解答:
解:(1)铁和氯化铜溶液反应生成氯化亚铁和铜,反应的化学方程式为Fe+CuCl2═FeCl2+Cu,离子方程式为Fe+Cu2+═Fe2++Cu,
故答案为:Fe+CuCl2═FeCl2+Cu;Fe+Cu2+═Fe2++Cu;
(2)除去FeCl2溶液中的FeCl3,可加入铁粉,反应的化学方程式为2FeCl3+Fe=3FeCl2,离子方程式为2Fe3++Fe=3Fe2+,
故答案为:2FeCl3+Fe=3FeCl2;2Fe3++Fe=3Fe2+.
故答案为:Fe+CuCl2═FeCl2+Cu;Fe+Cu2+═Fe2++Cu;
(2)除去FeCl2溶液中的FeCl3,可加入铁粉,反应的化学方程式为2FeCl3+Fe=3FeCl2,离子方程式为2Fe3++Fe=3Fe2+,
故答案为:2FeCl3+Fe=3FeCl2;2Fe3++Fe=3Fe2+.
点评:本题考查铁的性质,侧重于学生的分析能力的考查,注意把握物质的性质以及离子方程式的书写,难度不大,把握除杂的原理.

练习册系列答案
相关题目
光纤通讯是一种现代化的通讯手段,光纤通讯容量大,一对光纤上可同时传送3万门电话.制造光导纤维的主要原料是SiO2,下列关于SiO2的说法正确的是( )
| A、SiO2的摩尔质量是60 |
| B、1mol SiO2中含有1molO2 |
| C、1.5mol SiO2中约含有18.06×1023个氧原子 |
| D、1molSiO2的质量是60g/mol |
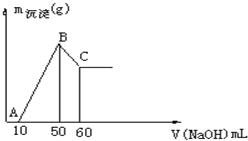 把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.合金中镁铝的物质的量之比为( )
把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.合金中镁铝的物质的量之比为( )| A、1:1 | B、1:2 |
| C、1:3 | D、2:1 |
能使水的电离平衡:H2O+H2O?H3O++OH-发生向电离的方向移动,且使溶液呈酸性的是( )
| A、在水中加KHCO3 |
| B、在水中加HCl |
| C、在水中加CuCl2 |
| D、将水加热至100℃ |