题目内容
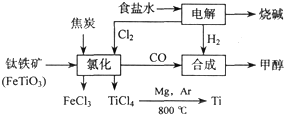
钛(Ti)被称为继铁、铝之后的第三金属,已知由金红石(TiO2)制取单质Ti,涉及的步骤为:![]()
已知①C(s)+O2(g) ![]() CO2(g);
CO2(g);
ΔH=-393.5 kJ·mol-1
② 2CO(g)+O2(g) ![]() 2CO2(g);
2CO2(g);
ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g)TiCl4(s)+O2(g);
ΔH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s) ![]() TiCl4(s)+2CO(g)的ΔH= 。
TiCl4(s)+2CO(g)的ΔH= 。
反应TiCl4+2Mg![]() 2MgCl2+Ti在Ar气氛中进行的理由是 。
2MgCl2+Ti在Ar气氛中进行的理由是 。
解析:根据盖斯定律,③+①×2-②,合并后得到反应式TiO2(s)+2Cl2(g)+![]() TiCl4(s)+2CO(g),则:ΔH=+141 kJ·mol-1+(-393.5 kJ·mol-1)×2-(-566 kJ·mol-1)=-80 kJ·mol-1。
TiCl4(s)+2CO(g),则:ΔH=+141 kJ·mol-1+(-393.5 kJ·mol-1)×2-(-566 kJ·mol-1)=-80 kJ·mol-1。
由于Mg、Ti在空气中高温下都有可能与空气中的O2(或CO2、N2)作用,故必须用Ar作保护气。
答案:-80 kJ·mol-1防止高温下Mg(或Ti)与空气中的O2(或CO2、N2)作用

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

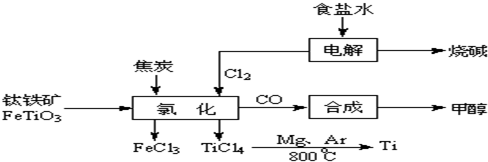
 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑ 2MgCl2(s)+Ti,在Ar气氛中进行的理由是:
2MgCl2(s)+Ti,在Ar气氛中进行的理由是: