题目内容
反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法错误的是( )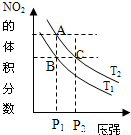
A.A、B、C三点中气体颜色最深的为C点
B.维持压强不变,由B点到A点反应向正方向进行
C.A、C两点的反应速率:A>C
D.B、C两点化学平衡常数:B<C
【答案】分析:N2O4(g)═2NO2(g)△H=+57kJ?mol-1,该反应为吸热反应,升高温度,化学平衡正向移动,NO2的体积分数增大,故温度T1<T2时,
A、根据温度、压强对平衡移动的影响,结合平衡移动原理分析解答;
B、A点NO2的体积分数大,压强相同,升高温度,化学平衡正向移动,NO2的体积分数增大;
C、A、C两点都在等温线上,压强越大,反应速率越快;
D、平衡常数只受温度影响,温度相同平衡常数相同.
解答:解:A.由图象可知,A、C两点都在等温线上,C点压强更大,故C点二氧化氮的浓度更大,颜色更深.由图可知A、B两点压强相等,A点二氧化氮的含量更大,A的浓度比B点浓度大,故C二氧化氮的浓度最大,颜色最深,故A正确;
B.升高温度,化学平衡正向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,由状态B到状态A,化学平衡正向移动,故B正确;
C.由图象可知,B、C两点都在等温线上,C的压强大,则A、C两点的反应速率:A<C,故C错误;
D.由图象可知,B、C两点所处的温度不同,C所处温度更高,升高温度平衡向正反应方向移动,平衡常数增大,故化学平衡常数KB<KC,故D正确;
故选C.
点评:本题考查化学平衡的图象,明确外界条件对化学平衡的影响及图象中纵横坐标的含义、“定一议二”“先拐先平”即可解答,难度不大.注意A选项为易错点,改变压强的本质为体积变化.
A、根据温度、压强对平衡移动的影响,结合平衡移动原理分析解答;
B、A点NO2的体积分数大,压强相同,升高温度,化学平衡正向移动,NO2的体积分数增大;
C、A、C两点都在等温线上,压强越大,反应速率越快;
D、平衡常数只受温度影响,温度相同平衡常数相同.
解答:解:A.由图象可知,A、C两点都在等温线上,C点压强更大,故C点二氧化氮的浓度更大,颜色更深.由图可知A、B两点压强相等,A点二氧化氮的含量更大,A的浓度比B点浓度大,故C二氧化氮的浓度最大,颜色最深,故A正确;
B.升高温度,化学平衡正向移动,NO2的体积分数增大,由图象可知,A点NO2的体积分数大,由状态B到状态A,化学平衡正向移动,故B正确;
C.由图象可知,B、C两点都在等温线上,C的压强大,则A、C两点的反应速率:A<C,故C错误;
D.由图象可知,B、C两点所处的温度不同,C所处温度更高,升高温度平衡向正反应方向移动,平衡常数增大,故化学平衡常数KB<KC,故D正确;
故选C.
点评:本题考查化学平衡的图象,明确外界条件对化学平衡的影响及图象中纵横坐标的含义、“定一议二”“先拐先平”即可解答,难度不大.注意A选项为易错点,改变压强的本质为体积变化.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
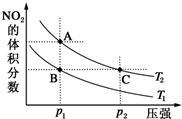 反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g)△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A、A、B两点的反应速率:A>B | B、B、C两点的反应平衡常数相同 | C、由状态B到状态C,可以用加热的方法 | D、A、C两点混合气体的平均相对分子质量:C>A |
 反应N2O4(g)?2NO2(g);△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
反应N2O4(g)?2NO2(g);△H=+57kJ?mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )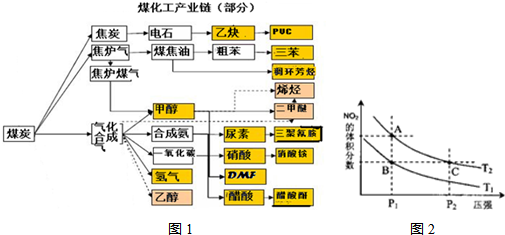
 和
和 .实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式
.实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式 对于反应N2O4(g)
对于反应N2O4(g) 2NO2(g)在温度一定时,平衡体系中NO2的体积分数ψ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是( )
2NO2(g)在温度一定时,平衡体系中NO2的体积分数ψ(NO2)随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点),下列说法正确的是( )