题目内容
下列变化需要加入适当的还原剂才能完成的是( )
| A、CuO→Cu |
| B、Fe→FeCl2 |
| C、H2SO3→H2SO4 |
| D、NO→NO2 |
考点:氧化还原反应
专题:
分析:需要加入还原剂才能实现,则选项中氧化剂在反应中元素的化合价降低,以此来解答.
解答:
解:A.Cu元素化合价降低,被还原,应加入还原剂,故A正确;
B.Fe元素化合价升高,被氧化,应加入氧化剂,故B错误;
C.S元素化合价升高,被氧化,应加入氧化剂,故C错误;
D.N元素化合价升高,被氧化,应加入氧化剂,故D错误.
故选A.
B.Fe元素化合价升高,被氧化,应加入氧化剂,故B错误;
C.S元素化合价升高,被氧化,应加入氧化剂,故C错误;
D.N元素化合价升高,被氧化,应加入氧化剂,故D错误.
故选A.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化解答的关键,侧重还原反应的考查,注意从化合价角度分析,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列化学用语书写正确的是( )
A、甲烷的电子式: |
B、丙烯的键线式: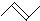 |
C、乙醚的结构式: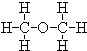 |
| D、乙烯的结构简式:CH2CH2 |
有X、Y、Z三种金属,把Y投入XCl2溶液中一段时间后,溶液质量增大,把Z投入YSO4溶液中一段时间后,溶液的质量减小,则这三种金属的还原性由强到弱的顺序正确的是( )
| A、X>Y>Z |
| B、Y>X>Z |
| C、Z>Y>X |
| D、Z>X>Y |
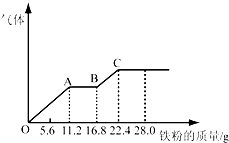 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示.下列分析或结果不正确的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示.下列分析或结果不正确的是( )| A、混合酸中HNO3物质的量浓度为2mol?L-1 |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、原混合酸中H2SO4物质的量为0.4 mol |
| D、第二份溶液中最终溶质为FeSO4 |
固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3、AgNO3中的一种或几种组成,某同学对该固体进行了如图实验:

下列判断正确的是( )

下列判断正确的是( )
| A、气体甲一定是纯净物 |
| B、白色沉淀甲可能是混合物 |
| C、固体X中一定存在AlCl3、(NH4)2SO4、MgCl2 |
| D、固体X中一定不存在FeCl2、AgNO3 |