题目内容
在850℃时,反应CO(g)+H2O(g)![]() CO2(g)+H2(g)+Q达到化学平衡,此时各物质的平衡浓度关系为:K=([CO2][H2])/([CO][H2O]),在850℃时,K=1,已知K值只与温度有关.试回答:
CO2(g)+H2(g)+Q达到化学平衡,此时各物质的平衡浓度关系为:K=([CO2][H2])/([CO][H2O]),在850℃时,K=1,已知K值只与温度有关.试回答:
(1)在850℃时,在2L密闭容器内,充入2molCO、2molH2O(g)进行上述反应,当达到平衡时,CO的转化率是________.
(2)在上述平衡体系中,充入6molH2O(g)后,平衡应向________移动,当达到新平衡时,CO的转化率又是________.
解析:
|
答案:50%;正反应方向;75% 分析:(1)CO(g)+H2O(g) C(始)1 1 0 0 C(转 x x x x C(平)1—x 1—x x x
CO的转化率:(0.5/1)×100%=50% (2)在CO(g)+H2O(g) CO(g)+H2O(g) C(始)0.5 6+0.5 0.5 0.5 C(转 y y y y C(平)0.5—y 6.5—y 0.5+y 0.5+y
此时,CO的转化率为[(3/8)÷0.5]×100%=75% |

 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案工业上制备H2的一种重要方法是:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=Q kJ·mol―1。已知该反应的平衡常数K与温度的关系如图所示。若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
CO2(g)+H2(g) △H=Q kJ·mol―1。已知该反应的平衡常数K与温度的关系如图所示。若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
|
| CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c4 |
| 4 | c1 | c2 | c3 | c4 |
已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是 。
A.单位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q 0(填“>”、“=”或“<”)。
(3)若在850℃时向反应容器中充入H2O(g),K值 (填“增大”、“减小”或“不变”,下同);若升高反应体系的温度,K值 。
(4)上表中c2为 mol·L=1,CO(g)的转化率为 。
工业上利用反应:CO(g)+H2O(g)![]() CO2(g)+H2(g);△H=Q kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。
CO2(g)+H2(g);△H=Q kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。
若在一容积固定的密闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
| t/min | CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c4 |
| 4 | c1 | c2 | c3 | c4 |
已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是_______.
A.单位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q______0(填“>”、“=”或“<”).
(3)若在850℃时向反应容器中充入H2O(g),K值_____(填“增大”、“减小”或“不变”).
(4)达平衡时CO2的反应速率______,CO(g)的转化率为_______.
工业上利用反应:CO(g)+H2O(g)  CO2(g)+H2(g);△H="Q" kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。
CO2(g)+H2(g);△H="Q" kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。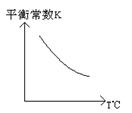
若在一容积固定的密 闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
| t/min | CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c4 |
| 4 | c1 | c2 | c3 | c4 |
已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是_______.
A.单
 位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
位时间内减少CO(g)的浓度等于生成CO2(g)的浓度B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q______0(填“>”、“=”或“<”).
(3)若在850℃时向反应容器中充入H2O(g),K值___
 __(填“增大”、“减小”或“不变”).
__(填“增大”、“减小”或“不变”). (4)达平衡时CO2的反应速率______,CO(g)的转化率为_______.
工业上利用反应:CO(g)+H2O(g)
 CO2(g)+H2(g);△H=Q kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。
CO2(g)+H2(g);△H=Q kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。

若在一容积固定的密闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
|
t/min |
CO(g) |
H2O(g) |
CO2(g) |
H2(g) |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c4 |
|
4 |
c1 |
c2 |
c3 |
c4 |
已知:850℃时该反应的化学平衡常数K=1.0,请回答下列问题:
(1)下列可以判断该反应达到化学平衡状态的是_______.
A.单位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
B.反应容器内的压强不发生变化
C.混合气体中H2(g)的浓度不再发生改变
D.氢气的生成速率等于水的消耗速率
(2)Q______0(填“>”、“=”或“<”).
(3)若在850℃时向反应容器中充入H2O(g),K值_____(填“增大”、“减小”或“不变”).
(4)达平衡时CO2的反应速率______,CO(g)的转化率为_______.
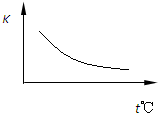 工业上制备H2的一种重要方法是:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q kJ?mol-1.已知该反应的平衡常数K与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质的浓度(mol?L-1)随时间的变化关系如下表:
工业上制备H2的一种重要方法是:CO(g)+H2O(g)?CO2(g)+H2(g)△H=Q kJ?mol-1.已知该反应的平衡常数K与温度的关系如图所示.若在一固定的密闭容器中,850℃时发生上述反应,并测得容器内各物质的浓度(mol?L-1)随时间的变化关系如下表: 时间/min
时间/min