题目内容
11.下列实验操作或实验事实与物质化学性质有关的是( )| A. | 用加热的方法分离碘和氯化钠固体 | |
| B. | 用水封的方法保存液溴 | |
| C. | 浓盐酸放置在空气中浓度减小 | |
| D. | 可以用氯水和四氯化碳鉴别Cl-、Br-、I- |
分析 A.加热时碘单质升华,属于物理性质;
B.由于溴在水中溶解度较小,所以保存液溴时使用水封;
C.浓盐酸具有挥发性,导致其浓度减小;
D.氯气能够氧化溴离子、碘离子,然后根据碘单质、溴单质在四氯化碳中的不同颜色可用鉴别.
解答 解:A.用加热的方法分离碘和氯化钠固体,利用的是碘单质的升华,属于物理性质,故A不选;
B.液溴具有挥发性,在水中的溶解度较小,所以保存液溴通常采用水封的方法,与溶解度有关,利用的是物理性质,故B不选;
C.浓盐酸放置在空气中浓度减小,原因是盐酸易挥发,属于物理性质,故C不选;
D.加入氯水和CCl4溶液,能生成I2、Br2,二者颜色不同,可鉴别三种离子,与物质化学性质有关,故D选;
故选D.
点评 本题考查化学实验方案的评价,题目难度不大,明确常见元素及其化合物性质为解答关键,注意掌握常见物质分离与鉴别方法,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
1. 美国海军海底战事中心与麻省理工学院共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )
美国海军海底战事中心与麻省理工学院共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )
 美国海军海底战事中心与麻省理工学院共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )
美国海军海底战事中心与麻省理工学院共同研制成功了用于潜航器的镁过氧化氢燃料电池系统.其工作原理如图所示.以下说法中错误的是( )| A. | 金属铂作电池的正极 | |
| B. | 电池的负极反应为Mg-2e-═Mg2+ | |
| C. | 电池总反应式是Mg+H2O2+2H+═Mg2++2H2O | |
| D. | 电池工作一段时间后,溶液的酸性增强 |
2.下列物质的结构简式中,书写正确的是( )
| A. | CH2CH2 | B. |  | C. | CH2=C(CH3)2 | D. | CH3COH |
19.某研究小组利用废弃的氧化铜锌矿(主要成分为CuO、ZnO、Fe2O3,还含有少量的CuS和ZnS等)制取活性ZnO,实验流程如图:

已知各离子开始沉淀及完全沉淀时的pH如下表所示:
回答下列问题:
(1)在“酸浸”步骤中,为提高浸出速率,可以采取的措施是粉碎矿石、搅拌、适当增大酸浓度适当升高温度;“浸渣”中只含有CuS,则相同温度下:Ksp(CuS)<(填“>”、“<”或“=”)Ksp(ZnS).
(2)酸浸后加入铁粉可发生多个反应,其中属于化合反应的化学方程式是Fe2(SO4)3+Fe═3FeSO4.
(3)除铁过程中物质A应使用下列物质中的b(填字母);该过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2≤pH<6.2范围之间.
a.KMnO4 b.H2O2 C.NaCIO
(4)证明Zn2(OH)2CO3已洗净的方法是取最后一次洗涤液,加入硝酸酸化的硝酸钡溶液,无沉淀生成,说明已洗净.
(5)在强碱性环境中,Fe(OH)3可被KCIO溶液氧化得到一种高效的多功能水处理剂K2FeO4.将除铁后得到的10.7g Fe(OH)3全部氧化,至少需要1mo1•L-l KC1O溶液150mL.

已知各离子开始沉淀及完全沉淀时的pH如下表所示:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.3 | 9.7 |
| Fe3+ | 1.4 | 3.2 |
| Zri2+ | 6.2 | 8.0 |
(1)在“酸浸”步骤中,为提高浸出速率,可以采取的措施是粉碎矿石、搅拌、适当增大酸浓度适当升高温度;“浸渣”中只含有CuS,则相同温度下:Ksp(CuS)<(填“>”、“<”或“=”)Ksp(ZnS).
(2)酸浸后加入铁粉可发生多个反应,其中属于化合反应的化学方程式是Fe2(SO4)3+Fe═3FeSO4.
(3)除铁过程中物质A应使用下列物质中的b(填字母);该过程中加入氨水的目的是调节溶液的pH,pH应控制在3.2≤pH<6.2范围之间.
a.KMnO4 b.H2O2 C.NaCIO
(4)证明Zn2(OH)2CO3已洗净的方法是取最后一次洗涤液,加入硝酸酸化的硝酸钡溶液,无沉淀生成,说明已洗净.
(5)在强碱性环境中,Fe(OH)3可被KCIO溶液氧化得到一种高效的多功能水处理剂K2FeO4.将除铁后得到的10.7g Fe(OH)3全部氧化,至少需要1mo1•L-l KC1O溶液150mL.
9.分子式为C9H12的苯的同系物,已知苯环上只有一个取代基,下列说法中正确的是( )
| A. | 该有机物不能发生取代反应,但能发生加成反应 | |
| B. | 该有机物苯环上的一溴代物最多有6种同分异构体 | |
| C. | 该有机物分子中的所有原子可能在同一平面上 | |
| D. | 该有机物不能使酸性的高锰酸钾溶液褪色,但能使溴水褪色 |
6.A原子的结构示意图为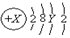 ,则X、Y及该原子3d能级上的电子数不可能的组合是( )
,则X、Y及该原子3d能级上的电子数不可能的组合是( )
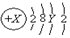 ,则X、Y及该原子3d能级上的电子数不可能的组合是( )
,则X、Y及该原子3d能级上的电子数不可能的组合是( )| A. | 18、8、0 | B. | 20、8、0 | C. | 25、13、5 | D. | 30、18、10 |
6. 室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )
 室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )
室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol•L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )| A. | 室温下,0.1 mol•L-1的三种酸溶液中由水电离产生的c(H+)的关系:HA>HB>HD | |
| B. | 滴定至P点时,溶液中c(B-)>c(Na+)>c(H+)>c(HB)>c(OH-) | |
| C. | pH=7 时,三种溶液中:c(A-)=c(B-)=c(D-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) |


 .
.
 .
. .
. (写结构简式).
(写结构简式).