题目内容
下列物质中属于非电解质的是
- A.氯化氢
- B.氯水
- C.铜
- D.二氧化碳
D
分析:根据非电解质、定义判断.
电解质:在水溶液里或熔融状态下能导电的化合物.
非电解质:在水溶液里或熔融状态下都不能导电的化合物.该概念的前提必须是化合物.
解答:A氯化氢是电解质,故A错误.
B氯水是混合物,故B错误.
C铜既不是电解质也不是非电解质,故C错误.
D、二氧化碳的水溶液能导电,但溶液中的离子是二氧化碳和水生成的碳酸电离的,而不是二氧化碳电离的,所以二氧化碳是非电解质,故D正确.
故选D.
点评:注意以下几点错误认识:
1、能导电的物质一定是电解质,如铜不是电解质但能导电.
2、电解质一定导电,如氯化钠晶体,因没有自由电子或自由离子,所以不导电.
3、不是电解质的物质就一定是非电解质,如氯气既不是电解质也不是非电解质.
4、其水溶液能导电的化合物是电解质,如二氧化硫,二氧化硫和水反应生成亚硫酸,亚硫酸电离出自由移动的离子,所以其水溶液能导电,因离子是亚硫酸电离的而不是二氧化硫电离的,所以二氧化硫是非电解质.
5、强电解质的水溶液导电能力强,如硫酸钡溶液,因硫酸钡难溶于水,所以其离子浓度很小,导电能力较差,但硫酸钡是强电解质.
分析:根据非电解质、定义判断.
电解质:在水溶液里或熔融状态下能导电的化合物.
非电解质:在水溶液里或熔融状态下都不能导电的化合物.该概念的前提必须是化合物.
解答:A氯化氢是电解质,故A错误.
B氯水是混合物,故B错误.
C铜既不是电解质也不是非电解质,故C错误.
D、二氧化碳的水溶液能导电,但溶液中的离子是二氧化碳和水生成的碳酸电离的,而不是二氧化碳电离的,所以二氧化碳是非电解质,故D正确.
故选D.
点评:注意以下几点错误认识:
1、能导电的物质一定是电解质,如铜不是电解质但能导电.
2、电解质一定导电,如氯化钠晶体,因没有自由电子或自由离子,所以不导电.
3、不是电解质的物质就一定是非电解质,如氯气既不是电解质也不是非电解质.
4、其水溶液能导电的化合物是电解质,如二氧化硫,二氧化硫和水反应生成亚硫酸,亚硫酸电离出自由移动的离子,所以其水溶液能导电,因离子是亚硫酸电离的而不是二氧化硫电离的,所以二氧化硫是非电解质.
5、强电解质的水溶液导电能力强,如硫酸钡溶液,因硫酸钡难溶于水,所以其离子浓度很小,导电能力较差,但硫酸钡是强电解质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



 ,③NaCl溶液,④Cu,⑤
,③NaCl溶液,④Cu,⑤ 固体,⑥纯蔗糖,⑦酒精,⑧熔融
固体,⑥纯蔗糖,⑦酒精,⑧熔融 ,⑨
,⑨ 气体,⑩
气体,⑩ 固体.
固体. ,③NaCl溶液,④Cu,⑤
,③NaCl溶液,④Cu,⑤ 固体,⑥纯蔗糖,⑦酒精,⑧熔融
固体,⑥纯蔗糖,⑦酒精,⑧熔融 ,⑨
,⑨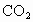 气体,⑩
气体,⑩ 固体.
固体.